Изменение - длина - связь
Cтраница 3
Отклонения от аддитивности энергий связей и изменения длин связей, наблюдаемые в молекулах с сопряженными связями, могут быть вызваны как делока-лизацией я-связей, так и различиями в гибридизации атомных орбит, служащих для образования а-связей. С-С образована атомами углерода в состоянии гибридизации хр3, а а-связь между атомами углерода 2 и 3 в бутадиене-1 3 - атомами в состоянии sp2, поскольку одна р-орбита каждого атома идет на образование л-связи. [31]
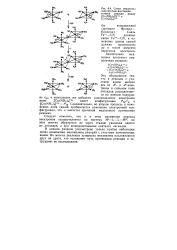 |
Схема механизма окислительно-восстановительной реакции между [ Со ( МН3 5С1 ] 2 и [ Сг ( Н20 6р. [32] |
Следовательно, во втором процессе к изменению длин связей прибавляется изменение электронной конфигурации, что и является причиной медленного протекания реакции. [33]
Поскольку резонансная стабилизация приводит обычно к изменениям длины связей и валентных углов, а также к изменениям гибридизации, влияние перегруппировок подобно резонансным эффектам. [34]
 |
Расстояние бор - азот в различных соединениях, пм. [35] |
Образование комплекса переноса заряда сопровождается и изменением длин связей. [36]
Очевидно, для установления зависимости между изменениями длин связей Fe - лиганд и кооперативными структурными событиями в определенной последовательности их протекания необходимо оценить стереохимические изменения координационного центра и его окружения относительно набора фиксированных координатных осей. В настоящее время невозможно точно определить последовательность кооперативных структурных событий, начинающихся с уменьшения радиуса катиона Fe ( II) при связывании кислорода и завершающихся изменением поверхностных контактов боковых цепей аминокислот ц - ( 32-субъединиц [99, 103], однако можно предположить вероятный механизм, по которому изменение ионного радиуса железа сказывается на структуре более отдаленных областей белка. [37]
Нетрудно видеть, что тенденция в изменении длин связей очень точно передается расчетом: связи С - С, находящиеся в соседстве с двойными связями ( например, в изобутилене), значительно сокращены по сравнению с простой связью С - С ( 1 51 - 1 52 А против 1 53 - 1 54 А); в перегруженных молекулах, таких, как гексаметилэтан, связи С - С существенно увеличены. При этом расхождение расчета и опыта в большинстве случаев не превышает нескольких сотых долей А. [38]
Даже после введения изменения р при изменении длины связи орбитали все еще сохраняют свойства, присущие орби-талям альтернантного углеводорода. Другими словами, энергии связывающей и разрыхляющей орбиталей все еще остаются симметричными относительно а, распределение заряда однородно, и орбитальные коэффициенты в соответствующих орби-талях связаны между собой таким же образом, как и раньше. Позднее будет видно, что свойства альтернантности, первоначально определенные в рамках метода Хюккеля, повторяются и в методе самосогласованного поля, в котором надлежащим образом учтены двухэлектронные взаимодействия и имеются недиагональные элементы гамильтониана, соответствующие взаимодействиям между электронами на орбиталях атомов, не являющихся ближайшими соседями. [39]
Как видно из табл. 8, интервал изменения длины связи Мо-Мо составляет 1 1 A, Re-Re 0 8 A, Rh-Rh, Pd-Pd, № - Ni, Си-Си 0 9 А. Варьирование межатомного расстояния в широких пределах, в общем, означает, что кривая энергии взаимодействия атомов в функции их расстояния имеет сравнительно пологий профиль с весьма размытым минимумом или серией из нескольких перекрывающихся минимумов. [40]
Хюккель [9], однако, отмечает, что изменение длины связи может быть обусловлено совместным действием различных факторов. Не подлежит сомнению, что в каждом частном случае один из ряда факторов может оказывать главное, определяющее влияние на длину связи, а остальные факторы будут играть лишь побочную, косвенную роль в изменении длины связи. [41]
При реализации вертикального способа стабилизации не требуется ни изменения длин связей стабилизирующей группы ( G), ни перемещения G к электронодефицитному центру I. [42]
Поэтому расчеты изменений длины связи С-С на основании изменений длин связей С - Н в зависимости от гибридизации [36] не оправданы. [43]
К сожалению, данные, позволяющие проследить за изменением длины связи Pd - PR3 и Pt - PR3 в зависимости от природы групп R, весьма ограничены и не очень убедительны. Однако, число исследованных структур rpaKC - M ( PR3hX2 невелико. [44]
Для того чтобы выяснить влияние изменения р при изменении длины связи на орбитальные энергии, мы рассмотрим решение задачи для бутадиена. Внешние связи С-С в бутадиене имеют длину 1 34 А, длина внутренней связи равна 1 48 А. Ранее было найдено, что для р следует принять значения 1 1р0 и 0 9р0 для внешних и внутренних связей соответственно. [45]
Страницы: 1 2 3 4