Изменение - константа - диссоциация
Cтраница 1
Изменение константы диссоциации при смене заместителя X определяется изменением электронной плотности на атоме углерода карбоксильной группы. [1]
По-видимому, это изменение констант диссоциации связано с уменьшением подвижности больших по размерам молекул диалкилсульфидов. Если насыщенная группа удаляется от атома серы, что имеет место в Р - и уненасыщенных соединениях, то атом серы лроявляет способность образовывать связь с йодом. [2]
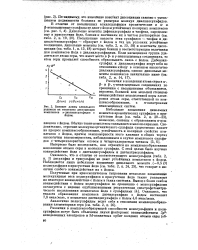 |
Влияние длины алкильного ненасыщенных систем. [3] |
По-видимому, это изменение констант диссоциаций связано с уменьшением подвижности больших по размерам молекул диалкилсульфидов. Насыщенные аналоги этих сульфидов - тиофан и ди-циклогексилсульфид - образуют с йодом в тех же. Если насыщенная группа удаляется от атома серы, что имеет место в Р - и уневасыщенных соединениях, то атом серы проявляет способность образовывать связь с йодом. [4]
Это является результатом изменения констант диссоциации и электронодонорных свойств лигандных групп ионита и главным образом возрастания жесткости полимерной сетки. Так, увеличение мольной доли мостикообра-зователяпри синтезе АН-40 снижает способность к координационному взаимодействию не только из-за уменьшения основности: расчет колебательных спектров длинных цепей поли-4 - винилпиридииа с применением метода нулевого приближения, сопоставление расчетных данных с экспериментальными ИК-спектрами сополимеров 4-ви-нилпиридина с различными количествами ДВБ показали, что при малых концентрациях мостикообразователя преимущественной будет спиральная конформация цепей между узлами сетки. Из ИК-спектров также следует, что скрученность участков цепей между поперечными связями с увеличением содержания ДВБ уменьшается, а затем, пройдя через минимум, снова повышается. [5]
Ниже приведены данные об изменении константы диссоциации аммиака в зависимости от температуры водной среды. [6]
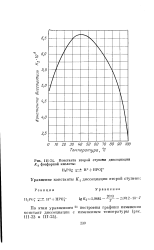 |
Константа второй ступени диссоциации К 2 фосфорной кислоты. [7] |
По этим уравнениям 24 построены графики изменения констант диссоциации с изменением температуры ( рпс. [8]
Это особенно резко проявляется при наблюдении за изменением константы диссоциации солей при переходе от растворителя к растворителю различных природных групп, например, при переходе от спиртов к растворителям, не содержащим гидроксильной группы. [9]
По мере увеличения длины цепи молекулы карбоновой кислоты изменение константы диссоциации при замене атома Н в w - положении на атом галоида становится все меньшим и меньшим. [10]
Следует заметить, что при этерификации фосфатов наблюдается изменение констант диссоциации фосфатных остатков. [11]
Различная адсорбируемость кислотных и основных компонентов на поверхности электрода приводит к изменению констант диссоциации адсорбированных кислот и оснований по сравнению с их величинами в объеме раствора. Его наряду с изменением приэлектродной концентрации заряженных веществ необходимо принимать во внимание при определении констант скорости приэлектродных поверхностных химических реакций. [12]
Другая сторона влияния постороннего электролита состоит в уменьшении диэлектрической проницаемости водной фазы, что приводит к изменению константы диссоциации реагента и константы устойчивости комплекса. Изменяются и константы распределения, которые зависят от ионной силы раствора. Суммарный результат действия солей предсказать довольно трудно. Физическая химия накопила значительный материал о коэффициентах активности неэлектролитов в растворах электролитов [52, 53], но эти данные учитывают не все стороны процессов, протекающих при экстракции внутрикомплекеных соединений. [13]
Из таблицы видно, что при наличии СН2 - группы между алкил-фенильной и карбоксильной группами в RC6H4CH2COOH изменение констант диссоциации зависит от индуктивного влияния алкильных групп. [14]
Если источником каталитически активного водородного иона является слабая кислота, то необходимо учитывать равновесие диссоциации слабого электролита и изменение константы диссоциации в зависимости от концентрации электролита, среды и температуры. Отсутствие количественных данных по константам диссоциации в неводных растворах тормозит изучение кислотного катализа в неводных средах. [15]
Страницы: 1 2 3