Изменение - константа - диссоциация
Cтраница 3
Влияние заместителей очень наглядно проявляется на изменении констант диссоциации ароматических кислот и фенолов. Отличие ароматических кислот от фенолов заключается в том, что в первых атом кислорода в анионе не находится в прямом полярном сопряжении с заместителем, а в фенолят-анионе имеется прямое полярное сопряжение, что приводит к значительно более сильному влиянию заместителей, особенно проявляющих - С-эффект. [31]
В случае электрофокусирования воздействие солей на изо-точку практически исключается, однако следует все же учитывать возможное влияние на белки сахарозы и амфолитов-носителей. Влияние сахарозы связано, вероятно, с изменением константы диссоциации аминогрупп белка вследствие более низкой диэлектрической постоянной среды. [32]
Атом фтора в стерическом отношении мало отличается от атома водорода, однако имеет существенно более высокую электроотрицательность. В связи с этим при введении фтора в аминокислоту наблюдается изменение константы диссоциации, причем этот эффект увеличивается по мере приближения места введения фтора к а-по-ложению аминокислоты. Трифторлейцин усваивается организмом вместо лейцина, тогда как 4 4 4-трифторвалин не усваивается вместо валина. Далее, в то время как 3 ( 3-дифторамфетамин присутствует в организме в виде свободного амина, незамещенный амфетамин присутствует преимущественно в протонированной форме. Если проанализировать распределение этих веществ в организме, можно видеть, что р ( 3-дифторамфетамин специфически усваивается жирами, причем метаболизм этого соединения осуществляется с участием реакции дезаминирования, тогда как амфетамин метаболирует в результате реакции гидроксилирования бензольного кольца. [33]
Декарбоксилирование в ряду пиридина в общем происходит значительно легче, чем Декарбоксилирование ароматических соединений. Легкость декарбоксилирования пиридинкарбоновых кислот понижается в порядке: пиколиновая-изоникотиновая-никотиновая, соответствующем изменению констант диссоциации этих кислот; константы диссоциации повышаются в том же ряду от пиколиновой кислоты к никотиновой. Это является прямым результатом понижения электронной плотности в положениях 2 и 4 пиридинового цикла. Относительная легкость декарбоксилирования пиридинкарбоновых кислот хорошо видна на примере декарбоксилирования хинолиновой и цинхомероновой кислот при нагревании: в обоих случаях главным продуктом реакции является никотиновая кислота. Дальнейшее Декарбоксилирование дает никотиновую кислоту ( XIII) с примесью небольшого количества изоникотиновой кислоты. [34]
Заметное влияние на получаемый результат, хотя и меньше, чем солевой состав, оказывает в отдельных случаях разница температур испытуемой воды и буфера. Отклонение температуры воды от ее температуры в водоеме и температуры буфера от 18 С вызывает изменение константы диссоциации индикатора. Стандартными условиями являются приведение рН воды к температуре ее в водоеме и приведение рН буфера к 18 С. [35]
Неточности определения рН могут зависеть от солевой ошибки, обусловленной высокой концентрацией солей в растворе, изменяющей растворимость и диссоциацию индикатора; от белковой ошибки, связанной с наличием в растворах белковых веществ ( кровь, плазма и др.); от индикаторной ошибки, так как белки, обладающие амфотерными свойствами, взаимодействуют с кислотными и основными индикаторами, а также адсорбируют индикатор; при этом происходит изменение общей концентрации его в испытуемом растворе; таким образом, добавление значительных количеств индикаторов, которые, являясь слабыми кислотами и основаниями, могут, особенно в незабуференных растворах, изменять значение рН; от температурной ошибки, зависящей от изменения константы диссоциации индикатора при колебаниях температуры; так, - нитрофенол имеет при 0е С рК - 7 30, а при 50 С р / С 6 81; с изменением температуры изменяется и рН стандартных растворов. [36]
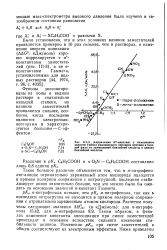 |
Корреляция а - констант с изменением энергии Гиббса равновесного переноса протона в газовой фазе от замещенной бензойной кислоты и аниону бензойной кислоты. [37] |
Ка я-нитрофенола меньше, чем рКа лг-нитрофенола, так как ь последнем нитрогруппа не находится в прямом полярном сопряжб нии с отрицательно заряженным атомом кислорода. Таким образом, в фенолах изменение константы диссоциации при смене заместителей происходит в основном вследствие сильного изменения стабильности анионов. Изменения рКа при смене заместителей в общем соответствуют их электронным эффектам. [38]
Зависимость констант диссоциации от температуры часто бывает немонотонной. Во многих случаях с ростом температуры константы диссоциации сначала возрастают, а затем уменьшаются. Тепловой эффект диссоциации кислот неодинаков, поэтому изменение констант диссоциации с температурой у разных кислот имеет разный характер и сила кислот, характеризуемая величиной рК, с температурой изменяется неодинаково. Нередко одна кислота более сильная, чем другая при 25 С, становится менее сильной, например, при 70 С. [39]
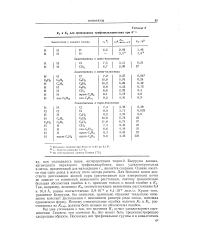 |
Для производных трифенилхлорметана при 0 а. [40] |
Бьеррума данных, касающихся перхлората трифенилкарбония, мало удовлетворительна и метод, примененный для нахождения г, является спорным. Однако имеется еще один довод в пользу этого метода расчета. Кроме того, уравнение Бьеррума, без сомнения, правильно отражает тенденцию изменения констант диссоциации с изменением размера ряда ионов, имеющих одинаковую форму. Поэтому относительные ошибки величин / С2 и / Сь рассчитанных из / ехр, должны быть меньше их абсолютных ошибок. [41]
В разбавленном растворе, в котором можно пренебречь солевым эффектом или учесть его, влияние растворителя, в основном, определяется уравнением ( VI. Значения коэффициентов активности myi, jcYi и sY отдельных ионных форм являются неопре-деленными. Грюнвальд с сотрудниками [37, 38] обосновывают возможность вычисления тун и отношения т А / тунА в водно-этаноль-ных средах наблюдаемой регулярностью в изменении констант диссоциации кислот НА двух типов заряда при постепенном переходе от чистой воды к чистому этанолу. Конечно, этот результат нельзя рассматривать как доказательство обоснованности таких вычислений. Более того, значения отношения т А / тУнА, найденные для карбоксильной кислоты или замещенного аммония, не позволяют оценить действие среды на индикатор сложного строения. Это заключение находится в согласии с содержанием предыдущих разделов настоящей главы. [42]
Величина константы диссоциации электролита, выражаемая уравнением типа (8.3) или (8.4), не изменяется при изменении концентрации. Например, уменьшение концентрации кислоты ( уменьшение знаменателя) приводит к уменьшению концентрации ионов ( уменьшение числителя), в связи с чем константа остается постоянной. Однако при значительном увеличении концентрации электролита ( при с 0 2 моль / л) число ионов в растворе увеличивается, сила взаимодействия их между собой и с растворителем возрастает, что вызывает некоторое изменение константы диссоциации. [43]
Страницы: 1 2 3