Изменение - константа - равновесие
Cтраница 2
Эти уравнения устанавливают связь между изменениями константы равновесия с температурой и тепловым эффектом реакции. Они относятся к процессам, протекающим при постоянном объеме, и называются уравнениями изохоры реакции. [16]
Представленные уравнения устанавливают связь между изменением константы равновесия с температурой и тепловым эффектом реакции. [17]
Это уравнение устанавливает связь между изменением константы равновесия с температурой и тепловым эффектом реакции, протекающей при постоянном объеме, и называется уравнением изохоры реакции. [18]
Это уравнение устанавливает связь между изменением константы равновесия с температурой и тепловым эффектом реакции, протекающей при постоянном объеме и называется уравнением изохоры реакции. [19]
Полученные уравнения устанавливают связь между изменением константы равновесия с температурой и тепловым эффектом реакции. Уравнения ( 238) и ( 239) относятся к условиям Р const и называются уравнениями изобары химической ре а к ц ии. Уравнения ( 240) и ( 241) относятся к условиям V const и называются уравнениями и з о х о р ы химической реакции. [20]
Эти уравнения устанавливают связь между изменением константы равновесия с температурой и тепловым эффектом реакции. [21]
Данное уравнение устанавливает связь между изменением константы равновесия с температурой и изохорным тепловым эффектом реакции. Оно называется уравнением изохоры химической реакции и применяется для процессов, протекающих при постоянном объеме. [22]
Эти уравнения устанавливают связь между изменениями константы равновесия с температурой и тепловым эффектом реакции. Они относятся к процессам, протекающим при постоянном объеме, и называются уравнениями изохоры реакции. [23]
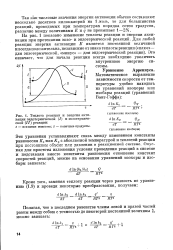 |
Теплота реакции и энергия активации эндотермической ( / и экзотермической ( / / реакций. 1 - исходные вещества. 2 - конечные продукты. [24] |
Эти уравнения устанавливают связь между изменением константы равновесия Кс или Кр с абсолютной температурой и теплотой реакции при постоянном объеме или давлении в реакционной системе. [25]
Уравнения изохоры и изобары реакции характеризуют изменение константы равновесия с температурой. Они определяют эту зависимость в дифференциальной форме. Для практических расчетов равновесия при различных температурах обычно необходимо бывает предварительно интегрировать их. [26]
Уравнения изохоры и изобары реакции характеризуют изменение константы равновесия с температурой. Они определяют эту зависимость в дифференциальной форме. Для практических расчетов равновесия при различных температурах требуется интегрирование этих уравнений. [27]
Уравнения изохоры и изобары реакции характеризуют изменение константы равновесия с температурой. Они определяют эту зависимость в дифференциальной форме. Для практических расчетов равновесия при различных температурах обычно необходимо бывает предварительно интегрировать их. [28]
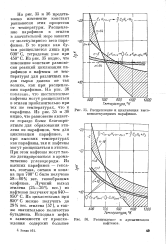 |
Расщепление и циклизация высокомолекулярных парафинов.| Расщепление и ароматизация нафтенов. [29] |
На рис. 35 и 36 представлено изменение констант равновесия этих процессов от температуры. Расщепление парафинов в этилен в значительной мере зависит от молекулярного веса парафинов. В то время как бутан расщепляется лишь при 600 С, тетрадекан уже при 450 С. Из рис. 35 видно, что изменение констант равновесия реакций циклизации парафинов в нафтены от температуры для различных видов сырья далеко не так велико, как при расщеплении парафинов. На рис. 36 показано, что шестичленпые нафтены могут расщепляться в этилен приблизительно при тех же температурах, что и парафины. Из рис. 35 и 36 видно, что равновесие является гораздо более благоприятным для образования этилена из парафинов, чем для циклизации парафинов, а при высоких температурах как парафины, так и нафтены могут расщепляться в этилен. При этом нафтены могут также дегидрироваться в ароматические углеводороды. Из высших парафинов - гекса-на, гептана, октана и нона-на при 700 С было получено 58 - 60 % вес. Лучший выход этилена ( 24 - 26 % вес. Из циклогексана при 850 С можно получить до 29 % вес. [30]
Страницы: 1 2 3 4