Изменение - константа - равновесие
Cтраница 3
Уравнения изохоры и изобары реакции характеризуют изменение константы равновесия с температурой. [31]
Уилмарт и Шварц [43] определили ряды изменения констант равновесия и констант скоростей образования геара-замещенныха а-дифенил - 3-бензоил-р - гидразилов из тетразанов в растворе ацетона при различных температурах, что позволило вычислить энергии и энтропии реакции и активации. X X Ю3 Дж / моль), а энтропия, как и следует ожидать для реакций дис-социации, сильно возрастает. Дж / моль), а энтропия активации гомолиза имеет небольшую отрицательную величину, поскольку обычно энтропия активации не учитывает изменения энтропии по координате реакции ( гл. Дж / моль) и что энтропия активации для этого процесса является сильно отрицательной, что обычно и наблюдается для реакций ассоциации ввиду значительных потерь в поступательной и вращательной энтропии. Основной причиной, обусловливающей сам факт наличия энергии активации процесса коллигации, является необходимость создания некоторой предварительной концентрации спиновой плотности на коллигирующихся атомах азота; на этот процесс оказывают влияние соседний атом азота и заместители. Влияние растворителя [40] на эти равновесные процессы будет значительно более сильным, чем влияние растворителя на равновесие гомолиза гексафенилэтана до трифенилметила ( разд. [32]
Эти уравнения показывают, что характер изменения константы равновесия однозначно определяется знаком теплового эффекта. В том случае, когда знак теплового эффекта положительный, производная логарифма константы равновесия по температуре больше нуля, а следовательно, функция 1п / С возрастает с повышением температуры. При отрицательном тепловом эффекте величина логарифма константы равновесия с повышением температуры убывает. [33]
Величина А Я может служить мерой изменения константы равновесия К ( точнее In / С) с температурой. Чем больше абсолютное значение ДЯ, тем сильнее / С зави-сит от температуры. Поэтому, если при Т 298 К КА Кв, то с повышением температуры разница будет еще больше увеличиваться, что приведет к росту отношения / Сл / / Св-Наоборот, при КА Кв рост температуры уменьшит разницу в кислотности, но отношение КА / КВ увеличится. При понижении же температуры указанное отношение уменьшится. [34]
Значения энтальпии обычно определяют либо по изменению константы равновесия с температурой, либо непосредственно калориметрически. При этом предпочтение отдается прямому калориметрическому методу. Метод, основанный на изучении зависимости IgK от 1 / Т, по-видимому, вполне пригоден для большинства реакций, сопровождающихся ионизацией протонного типа, так как подобные процессы обычно протекают в одну стадию, а величину р / С можно измерить с высокой степенью точности. Однако при комплек-сообразовании с металлами одновременно идет несколько реакций, в том числе сложных многоступенчатых процессов, включающих одну или несколько стадий протонной ионизации. Ошибки в определении р / С отдельных стадий суммируются, что значительно понижает точность измерений. Как правило, для реакций комплек-сообразования следует избегать определения ДЯ по температурной зависимости константы равновесия. Исключение составляют случаи, когда константа равновесия может быть измерена с очень высокой точностью, а также если есть возможность определить константы всех промежуточных стадий. [35]
Даже в химически индифферентных средах, где изменение константы равновесия обусловлено лишь влиянием диэлектрической проницаемости, растворитель может служить эффективным средством управления химическим равновесием. Сопоставляя константы равновесия процесса димеризации уксусной кислоты 2СНзСООНгс ( СНзСООН) 2, зависимость которых от обратной ДП приведена на рис. 1, с, можно рассчитать, что в 0 1 М растворе уксусной кислоты в w - гексане в димерной форме будет находиться примерно половина растворенной кислоты, в то время как в нитро-бензоловом растворе лишь около трети кислоты. [36]
В заключение полезно отметить, что величина изменения константы равновесия, индуцируемого связыванием субстрата, не ограничена значением константы равновесия для связывания самого субстрата, как это видно из следующих рассуждений. [37]
Выведенные термодинамические уравнения позволяют решить вопрос об изменении константы равновесия с температурой. [38]
Из выражения ( 73) следует, что изменение константы равновесия пропорционально разности приращений внутренней энергии исходных реагентов и продуктов реакции при наложении переменного электромагнитного поля. [39]
Нарушить установившееся равновесие могут факторы, приводящие к изменению константы равновесия, а также непосредственное изменение концентраций компонентов равновесия. [40]
Уравнения изохоры и изобары реакции позволяют производить количественные расчеты изменения константы равновесия при изменении температуры, если известна величина теплового эффекта реакции. Эти уравнения используются также для расчета теплового эффекта реакции по известной величине константы равновесия. Для получения расчетных формул необходимо уравнения ( VII, 11) и ( VII, 12) проинтегрировать. Интегрирование особенно просто в предположении, что тепловой эффект не зависит от температуры. Это предположение может быть принято без особых погрешностей для небольших интервалов температуры, пренебрегая небольшими температурными изменениями теплового эффекта. [41]
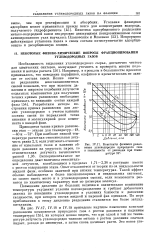 |
Константы фазового равновесия углеводородов природного газа в зависимости от давления при температуре 32. [42] |
На рис. IV.17, IV.18 и IV.19 приведены картины изменения констант равновесия компонентов природного газа с ростом давления и падением температуры [55], из которых можно видеть, что при одной и той же температуре летучесть углеводородов тяжелее метана с ростом давления сначала падает, доходя до минимума, а затем снова начинает расти. [43]
Ошибка в определении 3j величиной 2 пкал приводит к изменению константы равновесия в 3 раза. S приводит к изменению равн в 2 7 раза. [44]
Таким образом, изменение растворителя ведет прежде всего к изменению константы равновесия процессов, протекающих в растворе. [45]
Страницы: 1 2 3 4