Оксидное стекло
Cтраница 4
В работе [3] мы сделали попытку применить результаты теории МО, развитой для квадратных плоских комплексов Cu ( II) [5, 6] и комплексов ванадила симметрии Cit [2, 7], для оценки распределения спиновой плотности между центральным атомом и кислородными лигандами в оксидных стеклах. Как было отмечено выше, полученные нами экспериментальные результаты не противоречат исходным положениям этой теории. Вместе с тем автоматический перенос результатов работ [2-7 ] на изученные нами объекты сохраняет все недостатки, присущие данной теории, и привносит некоторые новые, связанные со спецификой оксидных стекол по сравнению с рассмотренными в теории примерами замороженных органических растворов. [46]
Термическая ширина запрещенной зоны, полученная из кривых температурного хода проводимости, в оксидных стеклах на основе Р2О5 V2O5 составляет 0 65 - 1 2 эв. В обычных оксидных стеклах с ионной проводимостью на основе SiO2 энергия активации колеблется в пределах 1 1 - 1 2 эв. [47]
Известно, что химические связи, действующие между атомами в упомянутых ранее окислах, частично являются ионными, а частично - ковалентными. Однако известны другие оксидные стекла, которые существуют благодаря водородным связям. Вероятно, к этой группе относится стеклообразный бисульфат калия. [48]
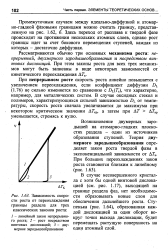 |
Зависимость скорости роста от переохлаждения. [49] |
При непрерывном росте скорость роста линейно повышается с увеличением переохлаждения, если коэффициент диффузии DL ( 1 76) не сильно изменяется по сравнению с DL ( Te), что характерно, например, для металлических систем. В случае оксидных стекол и полимеров, характеризующихся сильной зависимостью Z) L от температуры, скорость роста сначала увеличивается до максимума при некотором критическом значении АГкр, а затем при АГ АГкр уменьшается, стремясь к нулю. [50]
Стеклокерамика характеризуется существенно более высокими температурами деформации, чем стекла того же химического состава. Например, многие оксидные стекла имеют температуру стеклования Тяй 450сС, а размягчаются при 600 - 700 С. [51]
До сих пор мы рассматривали стекла, в которых межатомные связи, определяющие возможность структурной перегруппировки и тем самым устойчивость стекла, были частично или целиком ионными, как в нитратных и сульфатных системах. Чтобы завершить обзор группы оксидных стекол, рассмотрим стекла, структурной особенностью которых является присутствие водородных связей. Эти стекла образуются в ряде двойных систем, содержащих воду, структуру которой также определяют водородные связи. Далее будет также по казано, что существуют веские причины для того, чтобы включить в эту группу стекло K. [52]
И, наконец, все большее внимание привлекают к себе так называемые ионные полупроводники, электропроводность которых обусловлена переносом ионов, а не электронов. К таким полупроводникам относятся некоторые оксидные стекла, например, на основе SiO2 и многие другие полупроводники. [53]
Совсем недавно было найдено, что некоторые композиции в системе MgO - SisN могут быть получены в стеклообразном состоянии. Поскольку добавление небольших количеств нитрида в оксидные стекла ведет к повышению температуры стеклования Тк, новые стеклообразные материалы, содержащие большое количество нитрида кремния, могут также иметь весьма интересные свойства, например могут быть устойчивыми при высоких температурах. [54]
Если возможным и обычным является образование соединений переменного состава ( неопределенных соединений) между атомами, то еще более естественной кажется возможность образования неопределенных соединений между окислами, по крайней мере, в некоторых их сочетаниях. Примером этих соединений как раз и следует считать силикатные, боратные и другие оксидные стекла. [55]
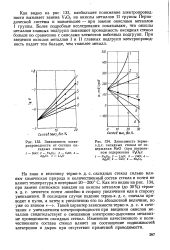 |
Зависимость электропроводности от состава оксидных стекол.| Зависимость термо-э. д.с. оксидных стекол от содержания МеО ( при постоянном содержании Р2Оь. [56] |
Как видно на рис. 133, наибольшее понижение электропроводности вызывает замена V2O5 на окислы металлов II группы Периодической системы и наименьшее - при замене окислами металлов I группы. Более подробные исследования показывают, что окислы металлов главных подгрупп понижают проводимость оксидных стекол больше по сравнению с окислами элементов побочных подгрупп. При введении окислов металлов I и II главных подгрупп электропроводность падает тем больше, чем тяжелее металл. [57]
Дано краткое обсуждение некоторых особенностей внедрения переходных ионов Cu ( II) и V ( IV) в структурную сетку оксидных стекол. За основу взяты экспериментальные результаты по изучению спектров ЭПР и электронного поглощения в бинарных оксидных стеклах и полученные на их основании оценки параметров химических связей в комплексах в приближении МО ЛКАО. Распределение спинолых плотностей внутри комплексов существенно зависит от матрицы стекла. [58]
Страницы: 1 2 3 4