Стеклообразование
Cтраница 2
Область стеклообразования в системе T1 - S, как видно на рис. 26, меньше области стеклообразования в системе Tl-Se. [16]
Область стеклообразования с таллием по-видимому, может быть расширена указанным образом от 50 до 100 % ( ат. [17]
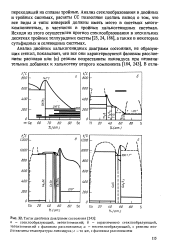 |
Типы двойных диаграмм состояния. [18] |
Анализ стеклообразования в двойных и тройных системах, расчеты СС позволяют сделать вывод о том, что все виды л типы инверсий должны иметь место в системах многокомпонентных, в частности в тройных халькогенидных системах. Исходя из этого осуществлен прогноз стеклообразования в нескольких десятках тройных теллуридных систем [23, 24,186], а также в некоторых сульфидных и селенидных системах. [19]
Процесс стеклообразования определяется следующими факторами: 1) внутренними, зависящими от природы веществ, находящихся в расплавленном состоянии; эти факторы стеклования расплавов связаны со строением атомов, входящих в состав расплава, и характером сил взаимодействия между ними; 2) внешними, зависящими от условий термообработки. Наиболее общим условием перехода в стеклообразное состояние является возможность переохлаждения расплава до таких температур, при которых вязкость расплава становится достаточно большой, достигая значений порядка 1013 Па-с. Очевидно, что расплав перейдет в стеклообразное состояние, если в процессе охлаждения в нем не возникнет ни одного зародыша кристаллизации, что исключает процесс кристаллизации полностью. [20]
 |
Область стеклообразования в системе As-S-Br. [21] |
Область стеклообразования в системе As-S-Br приведена на рис. 26.2 [28], где точка 3 имеет примерный состав Это стекло имеет температуру размягчения - 60 и при комнатной температуре обнаруживает текучесть воды. [22]
Условия стеклообразования, определяемые природой исходных веществ. Технология стекла долгие годы была ориентирована на получение стеклообразных веществ при определенных, практически достижимых реальных параметрах. [23]
 |
Удельное сопротивление стекол системы 13Na2O МеО2 ( Ме2О5 ( 87 - SiO2 при 150. [24] |
Область стеклообразования в системе Li2O - А12О3 - P2Os - SiOa отвечает составам ( в мол. [25]
Процесс стеклообразования протекает в 8 - 9 раз медленнее, чем силикатообразования. Это объясняется длительностью процесса растворения твердых зерен кварца в вязком расплаве силикатов и последующей диффузии растворенного вещества в глубь раствора. Оба процесса имеют разные скорости, и кинетика растворения зависит от соотношения этих скоростей. [26]
Скорость стеклообразования зависит от свойств растворяющегося вещества - кварцевых зерен и свойств растворителя - силикатного расплава. Она увеличивается с уменьшением величины зерен кварца, с отклонением формы зерен от шаровых, а также при наличии включений, нарушающих прочность кристаллической решетки кварца. Продолжительность стеклообразования сокращается с уменьшением вязкости расплава и его поверхностного натяжения, которые в свою очередь изменяются от состава стекол. [27]
Области стеклообразования в фосфатных системах с модифицирующими окислами РЬО, ZnO и CdO значительно шире, чем с окислами щелочных металлов. [28]
Область стеклообразования в системе As-S - Вг приведена на рис. 26.2 [28], где точка 3 имеет примерный состав Это стекло имеет температуру размягчения - 60 и при комнатной температуре обнаруживает текучесть воды. [29]
Процесс стеклообразования зависит от соотношения скорости охлаждения расплава ( которая определяет изменение вязкости) и скорости диффузионного перемещения атомов, при образовании упорядоченной кристаллической структуры. Если скорость изменения вязкости расплава сравнительно невелика, а ориентация атомов в равновесных положениях кристаллической решетки происходит быстро ( например, металлические жидкости), то стеклообразование отсутствует. Отсюда следует, что при достаточно быстром охлаждении можно получить даже металлические стекла. Действительно, при охлаждении металлических расплавов со скоростью около 106 град / мин были получены стеклообразные металлические пленки. [30]
Страницы: 1 2 3 4