Дисиликат - калий
Cтраница 1
Дисиликат калия K2Si2O5 может быть получен сплавлением поташа с кремнеземом, взятых в эквимолекулярных количествах. Кристаллы дисиликата калия гигроскопичны и хорошо растворяются в воде. Дисилдкат калия при высоких температурах легко сплавляется с SiO2, NaOH, КОН, взятых в произвольных количествах, образуя твердые растворы. [1]
Дисиликат калия ( K2O - 2SiO2) и тетрасиликат ( K2O - 4SiO2) образуют эвтектику состава 67 % SiO2 33 % K2O с температурой кристаллизации 742 С. Температура 742 С является наиболее низкой температурой появления расплава в системе. Есть сведения о существовании K2O - 3SiO2, что явилось основанием для изображения диаграммы состояния системы К2О - SiO2 с инконгруэнтно плавящимся при 800 С дисиликатом калия. [2]
Дисиликат калия кристаллизуется при охлаждении лишь с трудом; поэтому расплавы силиката калил обычно затвердевают в виде стекла. [3]
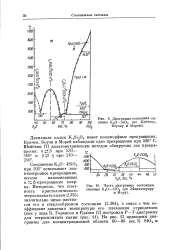 |
Диаграмма состояния системы К20 - Si02 ( по Крачеку, Боуэну и Морею.| Часть диаграммы состояния. [4] |
Дисиликат калия K2Si205 имеет полиморфные превращения. [5]
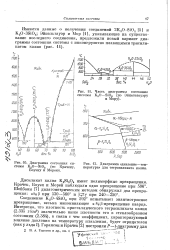 |
Часть диаграммы состояния.| Диаграмма состояния системы К20 - Si02 ( по Крачеку, Боуэну и Морею.| Диаграмма давление-температура для тетрасиликата калия. [6] |
Дисиликат калия KaSi2Os имеет полиморфные превращения. [7]
Безводные мета - и дисиликаты калия являются, по данным [1], соответственно цепочечными и слоистыми структурами с высокими температурами плавления. Безводный тетрасиликат представляет собой кольца из четырех кремнекислородных тетраэдров, которые соединены силоксановыми связями. Плотность этого соединения аномально низка, она меньше, чем плотность стекла того же состава. [8]
Инконгруентная частная система форстерит - лейцит - дисиликат калия имеет одно общее ребро с предыдущей системой: бинарную систему лейцит - форстерит. Точно так же ребро лейцит SijOs имеет простой бинарный характер, но частная система форстерит SizOs инконгруентна, и в ней образуется соединение К2О MgO 3SiO2 ( см. В. IL § 69), которое не имеет отношения к тройной частной системе. Шерер и Чап-пелир при решении этой сложной проблемы равновесия установили непрерывный подъем температуры от ее значений на ребре форстерит - дисиликат калия в поле К2О MgO 3SiO2 до температуры 1265 5 0 С, представляющей максимальную температуру, при которой форстерит и лейцит сосуществуют с этим соединением. Эта температура выше точки конгруентного плавления К2О MgO 3SiO2 ( 1134 2 C), Ввиду того что это интересное соединение весьма изоструктурно с кальсилитом, можно сделать предположение, что его поле в рассматриваемой тройной частной системе представляет кристаллические растворы типа кальсилита ( см. В. Две имеющиеся в системе точки пересечения определяют сосуществование лейцита, дисиликата калия, КаО MgO SSiOz, кристаллических растворов и расплава, а также лейцита, форстерита, кристаллических растворов и жидкости соответственно. [9]
Niggli [596], 84, 1913, 249) приготовили дисиликат калия, применив гидротермальный синтез. [10]
Те же условия имеют силу в случае кристаллизации и гидролиза моногидрата дисиликата калия, который - еще остается стабильным в присутствии воды при 285 С, но разлагается при несколько менее высокой температуре. Метасиликат калия и его гидраты подчиняются соответственному правилу: инвариантная точка с моногидратами мета - и дисиликата при 285 С отвечает отношению SiOj: К2О 1 13, а при 200 С это отношение уменьшается до 1 04 и стоит лишь незначительно снизить температуру, как это отношение станет менее 1 0, прячем метасиликат будет разлагаться водой. При таком разложении концентрационных соотношений системы кремнекислота - метасиликат калия - вода определенно не существует. Новые равновесные условия, представленные на фиг. [11]
В этой системе быстро кристаллизуются только смеси, лежащие между мета - и дисиликатом калия, и смеси, содержащие более 90 % кремнезема; в области же образования тетрасиликата калия К2Э 4SiOj преобладает затвердевание в виде стекла. Это соединение кристаллизуется с таким трудом, что только с помощью гидротермальных методов можно получить центры его кристаллизации и использовать их в качестве затравок для кристаллизации переохлажденных расплавов. Кри стобалит и тридимит легко кристаллизуются из богатых кремнеземом стекол после предварительной выдержки их в гидротермальных условиях, согласно правилу Оствальда; то же относится и к кварцу, который кристаллизуется позже в виде хорошо развитых кристаллов. [12]
При сопоставлении трех систем, исследованных Ниггли, можно видеть, что путем непосредственного сплавления ингредиентов могут быть непосредственно получены только дисиликат калия, метасиликат натрия и ортосиликат лития. Кривые равновесия в системах RzO - SiQ2 - СО2 довольно похожи друг на друга. [13]
Кривая растворимости одного полугидрата продолжается вплоть до значения отношения SiOj: KsO - 11 29, когда в качестве новой кристаллической фазы появляется дисиликат калия. [14]
Дисиликат калия K2Si2O5 может быть получен сплавлением поташа с кремнеземом, взятых в эквимолекулярных количествах. Кристаллы дисиликата калия гигроскопичны и хорошо растворяются в воде. Дисилдкат калия при высоких температурах легко сплавляется с SiO2, NaOH, КОН, взятых в произвольных количествах, образуя твердые растворы. [15]
Страницы: 1 2 3