Степень - ионность - связь
Cтраница 3
По этой причине невозможно рассчитать степень ионности связей металл - лиганд непосредственно по величине этого эффекта. Эти величины не слишком сильно отличаются от определенных другими способами значений степени ионности. [31]
В этом направлении возрастает также степень ионности связей в комплексных ионах, увеличивается радиус иона металла и число вакантных мест на d - орбиталях. [32]
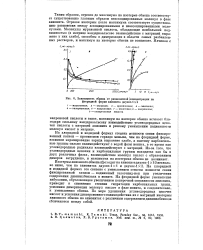 |
Зависимость обмена от равновесной [ концентрации на фторидной форме анионита дауэкс - 1х 2. [33] |
На хлоридной и иодидной формах степень ионности связи фиксированный катион - противоион гораздо меньше, чем на фторидной форме, взаимное экранирование заряда выражено слабо, а поэтому карбоксильные группы сильно взаимодействуют с водой фазы ионита, в то время как углеводородные радикалы взаимодействуют с матрицей. Из-за того, что углеводородные цепочки и карбоксильные группы находятся как бы в двух различных фазах, взаимодействие молекул кислот с образованием димеров затруднено, и максимума на изотермах обмена не возникает. [34]
 |
Электроотрицательность элементов.| Степень ионности некоторых связей. [35] |
В табл. 2 даны величины степени ионности связей кремния и углерода с некоторыми элементами. [36]
Кривая, показывающая зависимость между степенью ионности связи и разностью электроотрицательностей двух взаимосвязанных атомов. [37]
 |
Зависимость степени ионности связи Р от разности электроотрицатель-ностей х элементов по Полингу. [38] |
С увеличением разности электроотрицательностей элементов растет степень ионности связи. [39]
Одной из величин, количественно характеризующих степень ионности связи, является величина эффективного заряда иона. В настоящее время интенсивно разрабатываются методы определения эффективного заряда ионов в разных соединениях. Дипольный момент молекул SrO и ВаО был найден равным соответственно 8 9 и 7 9 D, что приводит к значению эффективного заряда ионов 0 97 и 0 85 заряда электрона вместо 2, как можно было бы ожидать, если бы связь была чисто ионной. [40]
 |
Зависимость степени нежности связи Р от разности электроотрицательностей элементов ( по Полингу. [41] |
С увеличением разности электроотрицательностей элементов растет степень ионности связи. [42]
Из правил Фаянса следует, что степень ионности связи в соединениях, образованных металлическими элементами и неметаллическими меняется так, как это показано на рис. 15.6. Электроположительные элементы в наибольшей степени проявляют ионность в соединениях с элементами правого верхнего угла Периодической таблицы, где располагаются кислород, фтор и хлор. [43]
 |
Электроотрицательность элементов по Полингу. [44] |
Из табл. 15.2 следует, что степень ионности связи С - Э меняется в широком интервале. Этот параметр, условно выражающий в процентах состояние ковалентной связи, промежуточное между неполярной ковалентной связью и чисто ионной связью. Он в значительной мере определяет свойства элементоорганических соединений. [45]
Страницы: 1 2 3 4