Степень - каустификация
Cтраница 3
Лабораторные исследования процесса разложения заводского феррита натрия, содержащего ib l % NaOH и 3 4 % Na2C03, при степени каустификации 87 1 %, проведенные при различных температурах и постоянном времени выщелачивания ( 2 сут), достаточном для получения равновесных растворов, показали, что чем выше температура выщелачивания, тем больше содержание NaOH в конечном растворе. [31]
По окончании всех опытов полученные образцы феррита ( каждый в отдельности) выщелачивают водой и определяют выход едкого натра, или степень каустификации соды, с целью проверки общего выхода реакции, установленного ранее по количеству выделившегося углекислого газа. [32]
Это выражение показывает, что равновесие в рассматриваемой системе определяется исключительно соотношением рас-творимостей гидроокиси и карбоната кальция и указывает пути повышения равновесного выхода NaOH, называемого степенью каустификации. [33]
При текущем контроле в суспензии, выходящей из гасителя-каустификатора, определяют избыток активной извести и содержание NaOH и Na2COs в прозрачной части суспензии; по последним двум определениям рассчитывают степень каустификации. [34]
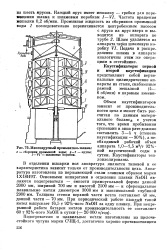 |
Многоярусный промывателъ шлама. [35] |
Объем каустификаторов зависит от производительности цеха и может быть рассчитан по данным материального баланса с учетом того, что время пребывания суспензии в аппа рате должно составлять 3 - 4 ч ( степень каустификации - 90 %), а необходимый рабочий объем аппарата 1 0 - 1 5 м3 / т 92 % - ной каустической соды в сутки. [36]
Условия равновесия определяются соотношением между растворимостями гидроокиси и карбоната кальция. Степень каустификации возрастает с уменьшением концентрации соды в исходном растворе ( рис. 68) и с понижением температуры. Однако на практике процесс осуществляют при 80 - 100 С с целью увеличения скорости взаимодействия реагентов и получения крупнокристаллического осадка карбоната кальция. [37]
Условия равновесия определяются соотношением между растворимостями гидроокиси и карбоната кальция. Степень каустификации возрастает с уменьшением концентрации соды в исходном растворе и с понижением температуры. Однако на практике процесс проводят при 80 - 100 С для увеличения скорости взаимодействия реагентов и получения крупнокристаллического осадка карбоната кальция. [38]
Условия равновесия определяются соотношением между растворимостями гидроокиси и карбоната кальция. Степень каустификации возрастает с уменьшением концентрации соды в исходном растворе ( рис. 68) и с понижением температуры. Однако на практике процесс осуществляют при 80 - 100 С с целью увеличения скорости взаимодействия реагентов и получения крупнокристаллического осадка карбоната кальция. [39]
При выщелачивании феррита в последних по ходу жидкости выщелачивателях Na2CO3 обычно выпадает в осадок, так как ее растворимость снижается с повышением концентрации NaOH. При уменьшении степени каустификации ниже нормы количество кристаллизующейся соды может быть настолько велико, что выщелачиватель забивается и нормальная работа его нарушается. [40]
По окончании опыта мешалку выключают и каусти-цер вынимают из термостата. Для определения степени каустификации отфильтровывают шлам, промывают осадок и определяют содержание NaOH и Na2CO3 отдельно в фильтрате и в промывных водах. [41]
По полученным аналогичным данным рассчитывают степень каустификации для каждого опыта, а также выход едкого натра в процентах от теоретически возможного. Примерный расчет степени каустификации приведен ниже. Затем изображают графически зависимость степени каустификации от температуры или концентрации исходного содового раствора. [42]
Полученный фильтрат охлаждают, доводят объем в мерной колбе до метки и анализируют его на содержание едкого натра и углекислого натрия. По результатам опытов рассчитывают степень каустификации и выход продуктов реакции по отношению к максимально возможному. [43]
При выполнении работы устанавливается 1) зависимость степени каустификации от концентрации соды в исходном растворе; 2) зависимость скорости каустификации от температуры. По результатам работы строятся кривые зависимости степени каустификации от времени при различных температурах. [44]
При концентрации соды в растворе выше 23 2 масс. % в донной фазе появляется пирсонит Na2C03 - CaCO3 - 2H20, способствующий возрастанию потерь соды. Наоборот, при понижении концентрации соды в исходном растворе степень каустификации повышается. [45]
Страницы: 1 2 3 4