Степень - перекрывание - электронное облако
Cтраница 3
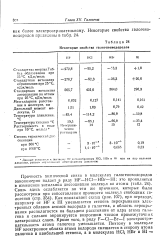 |
Некоторые свойства галогеноводородов. [31] |
Связь здесь ослабляется по тем же причинам, которые были рассмотрены при сопоставлении прочности молекул свободных галогенов ( стр. Как показывает схема ( рис. 107), при переходе, например от HF к HI уменьшается степень перекрывания электронных облаков атомов водорода и галогена, а область перекрывания располагается на большем расстоянии от ядра атома галогена и сильнее экранируется возросшим числом промежуточных электронных слоев. Кроме того, в ряду F - С1 - Вг-I электроотрн - - цательность атома галогена уменьшается. [32]
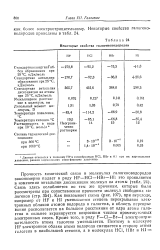 |
Некоторые свойства галогеноводородов. [33] |
Связь здесь ослабляется по тем же причинам, которые были рассмотрены при сопоставлении прочности молекул свободных галогенов ( стр. Как показывает схема ( рис. 107), при переходе, например от HF к HI уменьшается степень перекрывания электронных облаков атомов водорода и галогена, а область перекрывания располагается на большем расстоянии от ядра атома галогена и сильнее экранируется возросшим числом промежуточных электронных слоев. Кроме того, в ряду F - С1 - Вг-I электроотрицательность атома галогена уменьшается. [34]
Связь здесь ослабляется по тем же причинам, которые были рассмотрены при сопоставлении прочности молекул свободных галогенов ( стр. Как показывает схема ( рис. 107), при переходе, например, от HF к HI уменьшается степень перекрывания электронных облаков атомов водорода и галогена, а область перекрывания располагается на большем расстоянии от ядра атома галогена и сильнее экранируется возросшим числом промежуточных электронных слоев. Кроме того, в ряду F - С1 - Вг-I электроотрицательность атома галогена уменьшается. Поэтому в молекуле HF электронное облако атома водорода смещается в сторону атома галогена в наибольшей степени, а в молекулах НС1, НВг и HI - все меньше и меньше. Это также приводит к уменьшению перекрывания взаимодействующих электронных облаков и, тем самым, к ослаблению связи между атомами. [35]
 |
Схема перекрывания электронных облаков при образовании молекул HF и HI. [36] |
Связь здесь ослабляется по тем же причинам, которые были рассмотрены при сопоставлении прочности молекул свободных галогенов ( стр. Как показывает схема ( рис. 107), при переходе, например, от HF к HI уменьшается степень перекрывания электронных облаков атомов водорода и галогена, а область перекрывания располагается на большем расстоянии от ядра атома галогена и сильнее экранируется возросшим числом промежуточных электронных слоев. Кроме того, в ряду F - С1 - Вг - I электроотрицательность атома галогена уменьшается. Поэтому в молекуле HF электронное облако атома водорода смещается в сторону атома галогена в наибольшей степени, а в молекулах НС1, НВг и HI - все меньше и меньше. Это также приводит к уменьшению перекрывания взаимодействующих электронных облаков и, тем самым, к ослаблению связи между атомами. [37]
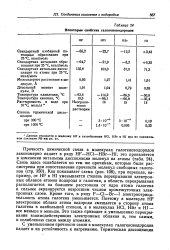 |
Некоторые свойства галогеноводородов. [38] |
Связь здесь ослабляется по тем же причинам, которые были рассмотрены при сопоставлении прочности молекул свободных галогенов ( стр. Как показывает схема ( рис. 108), при переходе, например, от HF к HI уменьшается степень перекрывания электронных облаков атомов водорода и галогена, а область перекрывания располагается на большем расстоянии от ядра атома галогена и сильнее экранируется возросшим числом промежуточных электронных слоев. Кроме того, в ряду F - С1 - Вг-I электроотрицательность атома галогена уменьшается. Поэтому в молекуле HF электронное облако атома водорода смещается в сторону атома галогена в наибольшей степени, а в молекулах HCI, НВг и HI - все меньше и меньше. Это также приводит к уменьшению перекрывания взаимодействующих электронных облаков и, тем самым, к ослаблению связи между атомами. [39]
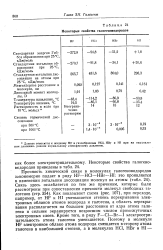 |
Некоторые свойства галогеноводородов. [40] |
Связь здесь ослабляется по тем же причинам, которые были рассмотрены при сопоставлении прочности молекул свободных галогенов ( стр. Как показывает схема ( рис. 107), при переходе, например, от HF к HI уменьшается степень перекрывания электронных облаков атомов водорода и галогена, а область перекрывания располагается на большем расстоянии от ядра атома галогена и сильнее экранируется возросшим числом промежуточных электронных слоев. Кроме того, в ряду F - С1 - Вг-I электроотрицательность атома галогена уменьшается. [41]
 |
Некоторые комплексы металлов в МВС. [42] |
Освобождающиеся электронные орбитали участвуют в образовании г-связей с лигандами. В табл. 14 собственные электронные пары комплексообразователя изображены сплошными стрелками, а электронные пары лигандов, ответственные за донорно-акцепторные сг-связи, - пунктирными стрелками. Степень перекрывания электронных облаков при этом меньше и связь лигандов с комплексообразовате-лем слабее, чем при внутренней гибридизации. Co ( NH3) 6 ] 3, в котором гибридизация внутриорбитальная. Приведенные в табл. 14 электронные структуры комплексов правильно отражают их магнитные свойства. Так, [ Cu ( NH3) 2 ], [ Zn ( NH3) 4 ] 2, [ Ni ( CN) 4 ] 2 -, [ Co ( NH3) 6p диамагнитны: у них нет неспаренных электронов. В противоположность им [ NiCl4 ] 2 и [ CoF6 ] 3 парамагнитны. При этом парамагнетизм этих соединений пропорционален числу неспаренных электронов. [43]
 |
Некоторые комплексы металлов в МВС. [44] |
Освобождающиеся электронные орбитали участвуют в образовании ег-связей с лигандами. В табл. 14 собственные электронные пары комплексообразователя изображены сплошными стрелками, а электронные пары лигандов, ответственные за донорно-акцепторные сг-связи, - пунктирными стрелками. Степень перекрывания электронных облаков при этом меньше и связь лигандов с комплексообразовате-лем слабее, чем при внутренней гибридизации. Поэтому в комплексе [ CoF6 ] s - замещение ионов фтора идет легко и он более реакционноспособен, чем [ Co ( NHg) 6 ] 3, в котором гибридизация внутриорбитальная. Приведенные в табл. 14 электронные структуры комплексов правильно отражают их магнитные свойства. Так, [ Cu ( NH3) 2 ], [ Zn ( NH3) 4p, [ Ni ( CN) 4p -, [ Co ( NH3) 6 ] 3 диамагнитны: у них нет неспаренных электронов. В противоположность им [ NiClt ] 2 - и [ CoF6 ] 3 парамагнитны. При этом парамагнетизм этих соединений пропорционален числу неспаренных электронов. [45]
Страницы: 1 2 3 4