Высшая степень - окисление
Cтраница 1
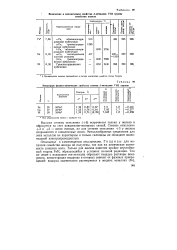 |
Некоторые физико-химические свойства атомов d - металлов VIII группы. [1] |
Высшая степень окисления ( 6) встречается только у железа и образуется за счет ковалентно-полярных связей. Степень окисления 3 и 2 - связи ионные, но для степени окисления 3 у железа сохраняются и ковалентные связи. Металлообразные соединения для этих металлов не характерны и только силициды их обладают значительной электропроводностью. [2]
 |
Некоторые свойства марганца, технеция, рения. [3] |
Высшая степень окисления 7 обусловлена образованием связей с помощью всех s - и d - элек-тронов. [4]
 |
Свойства металлов VB-группы. [5] |
Высшая степень окисления этих металлов 5 достигается за счет потери атомами s - электронов внешнего и d - электронов предпоследнего уровня. Более низкие степени окисления 4, 3 и 2 характерны главным образом для ванадия. [6]
Высшая степень окисления - это наибольшее для данного элемента положительное значение степени окисления. Она всегда равна номеру группы периодической системы и является важной количественной характеристикой элемента в его соединениях. Наименьшее значение степени окисления элемента, которое встречается в его соединениях, принято называть низшей степенью окисления. Все остальные встречающиеся степени окисления атома элемента называют средними или промежуточными. [7]
 |
Растворимость водорода в железе и никеле в зависимости от температуры ( рн 1 013 105 Ли2. [8] |
Высшая степень окисления ( 6) встречается только у железа и образуется за счет ковалентно-полярных связей. Степень окисления 3 и 2 - связи ионные, но для степени окисления 3 у железа Сохраняются и ковалентные связи. [9]
Высшие степени окисления As2O5 и Sb2C5 действуют окислительно, отдавая часть своего кислорода. [10]
 |
Строение иона IO2Fjr. [11] |
Высшая степень окисления 7 характерна для иода. Для него известны гептафторид IF, триооксофторид IO3F и производные тет-раоксоиодат - [ Ю41 - и, гексаоксоиодат [ Ю6 ] 6 - - комплексов. [12]
Высшая степень окисления ( VIII) устойчива у осмия в таких соединениях, как тетраоксид осмия OsO4 и тетраоксодиакваосмий [ Os ( H2O) 2C4 ]; последний обладает кислотными свойствами в водном растворе. [13]
Высшая степень окисления (, V) для азота и висмута неустойчива. [14]
Высшая степень окисления у висмута неустойчива и соединения висмута ( V), на уимгр висмута. [15]
Страницы: 1 2 3 4