Высшая степень - окисление
Cтраница 2
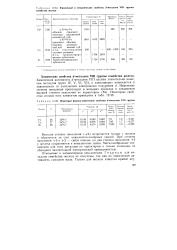 |
Некоторые физико-химические свойства d - металлов VIII группы. [16] |
Высшая степень окисления ( 6) встречается только у железа и образуется за счет ковалентно-полярных связей. При степени окисления 3 и 2 - связи ионные, но для степени окисления 3 у железа сохраняются и ковалентные связи. Металлообразные соединения для этих металлов не характерны и только силициды их обладают значительной электрической проводимостью. [17]
 |
Свойства металлов VB-подгруппы. [18] |
Высшая степень окисления этих металлов 5 достигается за счет потери атомами s - электронов внешнего и d - электронов предпоследнего уровня. Более низкие степени окисления 4, 3 и 2 характерны главным образом для ванадия. [19]
 |
Степени окисления атомов степень окисления совпадает с номе. [20] |
Высшая степень окисления неметаллов обычно равна НГ, особенно в соединениях с кислородом. [21]
Высшая степень окисления ванадия стабилизируется в фторо - и оксопроизводных. [22]
Высшая степень окисления ванадия стабилизируется в фторо - и оксопроизвод-ных. [23]
Высшая степень окисления V для азота и висмута неустойчива. Соединения висмута ( У) проявляют окислительные свойства, особенно сильные в кислотной среде. Переход от висмута ( Ш) к производным висмута ( У) происходит только под действием очень сильных окислителей и в щелочной среде. [24]
 |
Свойства металлов VI группы побочной подгруппы. [25] |
Высшие степени окисления рения более устойчивы, чем марганца. [26]
Высшей степени окисления мышьяка и сурьмы соответствуют соединения, в которых их атомы находятся в состоянии sp3 -, sp3d - или зр3сР - гибридизации. [27]
Однако высшие степени окисления для Ри менее характерны. [28]
Поэтому высшая степень окисления для Sc равна 3, и она увеличивается на единицу в каждой следующей группе, достигая максимального значения 7 у Мп. После этого степень окисления вновь уменьшается на единицу у каждого следующего металла ( Fe, Co, Ni, Си), достигая 2 у Zn. Единственным исключением из этого правила является отсутствие степени окисления 5 у Со. Эта особенность Со будет объяснена в гл. [29]
Однако высшие степени окисления для Ри менее характерны. [30]
Страницы: 1 2 3 4