Стереонаправленность
Cтраница 1
Стереонаправленность имеет огромное значение при разработке синтеза природных соединений. Кроме того, она стала играть чрезвычайно важную роль в синтезе некоторых полимеров, строго упорядоченная молекулярная архитектура которых придает им особые, часто весьма желательные физические свойства. Несмотря на очевидное практическое значение этих вопросов, в рамках учебника они могут быть изложены только вкратце. Стереонаправленный синтез подобно синтезу вообще все еще является искусством, которому нельзя научить в полном смысле этого слова. Можно сформулировать определенные принципы и показать, каким образом их использовали, но применение этих принципов для решения новых задач все еще требует значительной оригинальности и изобретательности. Стереорегулярная полимеризация на практике представляет собой искусство в еще большей степени. Хотя в настоящее время существует довольно ясная картина в отношении природы стереорегулярных полимеров, однако имеется много разногласий по поводу способа их образования, и, по-видимому, до сих пор существует мало оснований для предсказаний, даст или не даст новая система катализаторов исключительно стереорегуляр-ный полимер. [1]
Стереонаправленность диенового синтеза определяется правилом г мс-присоединения ( диеновый синтез идет по схеме г мс-присоединения диена к диено-филу) и правилом накопления ненасыщенности ( конфигурация получающегося аддукта определяется стремлением образующейся в нем двойной связи расположиться в пространстве ближе к ненасыщенной активирующей группе диенофила), напр. [2]
Стереонаправленность реакции Виттига зависит от условий ее проведения: в кинетически контролируемых условиях ( при низкой температуре, в полярных апротонных растворителях, в присутствии оснований Льюиса или при отсутствии карбоанионной стабилизации метилидной части молекулы) происходит немедленная циклизация промежуточного биполярного иона, и реакция идет как формальное [2 2] - циклоприсоединение. Промежуточное циклическое соединение сохраняет пространственную ориентацию заместителей, существовавшую в момент сближения реагентов; такая ориентация отвечает цис-расположеняю заместителей. [3]
Причина стереонаправленности перициклических процессов может быть объяснена по Вудворду и Гофману с позиций ранее ими высказанного принципа сохранения орбитальной симметрии при синхронных реакциях. Наиболее простое понимание можно получить, если схематически представить молекулярные орбитали электронных систем как линейную комбинацию атомных орбита-лей ( метод ЛКАО Хюккеля); при построении молекулярных ор-биталей следует иметь в виду, что электроны молекулярной я-электронной орбитали, охватывающей п атомов, могут быть расположены на / г-связывающих или Д - разрыхляющих орбиталях и что при сигматропных перегруппировках я-электроны, возникающие при разрыве 0-связи так же, как и я-электроны, участвующие в образовании а-связи, находятся в молекулярной орбитали как я-электроны. На рис. II-1 представлены молекулярные орбитали разной энергии для четырех-я-электронной ( бутадиена) и шестиэлектронной ( гексатриена) систем. [4]
 |
Образование транс - 1 2-диметилциклогексана при гидрировании. [5] |
Несомненно, стереонаправленность при гидрировании алкилфенолов невелика, и трудно предсказать, какой продукт будет преобладать. Положение дополнительно осложняется тем, что в некоторых случаях в качестве промежуточных продуктов могут образовываться алкилциклогексаноны. Восстановление этих кетонов мы уже рассмотрели в разд. [6]
Что касается стереонаправленности реакций, в том числе возможностей асимметрического синтеза с высокой энантио-селективностью, то это объясняется высоким матричным эффектом МФК - искуственно вводимыми хиральными индукторами на поверхности раздела фаз. [7]
Поскольку наблюдаемую экспериментально стереонаправленность стадии передачи цепи трудно было объяснить влиянием заместителей в плоскости радикального центра, авторы [138] предположили, что для замещения с CCU и, вероятно, присоединения к пропилену важную роль играет асимметрическая индукция ближайших к растущему концу хиральных центров. [8]
 |
Стереохимия гидроборирования. [9] |
Точное определение понятий стереонаправленности и стереоспецифичности дано в гл. [10]
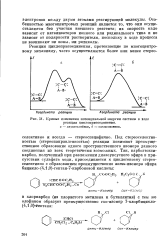 |
Кривые изменения потенциальной энергии системы в ходе реакции циклоприсоединения. [11] |
Под стереоселектив-ностью ( стереонаправленностью) реакции понимают преимущественное образование одного пространственного изомера данного соединения из всех теоретически возможных. [12]
Голд [53] объясняет такую стереонаправленность механизмом, включающим образование я-комплекса XLIX, однако здесь имеется ряд неопределенностей. Одна из них состоит в том, что присоединение может инициироваться протоном при карбоксильном атоме кислорода. [13]
Отдельно следует остановиться на стереонаправленности восстановления оптически активных соединений. [14]
Данные экстраполяции свидетельствуют о высокой стереонаправленности этой реакции. Преимущественное образование цис-i 2-диметилциклогексана также связано с образованием неклассического 1 1-димети. [15]
Страницы: 1 2 3