Стереонаправленность
Cтраница 3
 |
Состав продуктов изомеризации дициклопентила как функция степени превращения исходного углеводорода. [31] |
Дициклопентил испытывает превращение в декалин. Реакция идет с сохранением числа третичных атомов углерода и принадлежит к числу относительно быстрых превращений. Особенно следует отметить стереонаправленность этой реакции, достигающую величины порядка 85 % ( см. рис. 75), причем первичным продуктом реакции является термодинамически менее устойчивый уыс-дека-лин. [32]
Так, гидрирование двойной связи в 1 -бензилоксикарбонил - 4-пропилиденпирролидин - 2-карбоновой кислоте на платиновом катализаторе приводит в основном к образованию t / ноизомера. Следовательно, эта непредельная кислота в ходе реакции адсорбируется на катализаторе большей частью таким образом, что ее карбоксильная группа обращена в сторону, противоположную поверхности катализатора. Чтобы изменить положение молекулы кислоты на катализаторе при адсорбции и тем самым стереонаправленность гидрирования, используют в качестве носителя катализатора не нейтральный пористый материал, как обычно, а основную ионообменную смолу. Благодаря солеобразованию с такой подложкой карбоксильная группа начинает играть роль своего рода якоря, ориентирующего адсорбирующуюся молекулу карбоксильной группой вниз, к поверхности катализатора. [33]
Описан метод [3] определения положения атомов дейтерия, присоединенных к циклогексановым кольцам. Полученные данные показывают, что для дифференциации между аксиальными и экваториальными ориентациями дейтерия в производных цик-логексана может быть использован метод инфракрасной спектроскопии. Соответствующие исследования проводили с указанными ниже стероидами, которые были помечены в определенных положениях с использованием реакций, характеризующихся заведомо известной стереонаправленностью. [34]
Подобное действие оказывают также два заместителя. Например, показано [195], что г с-3 - метил-4 - ацетоксиметилциклогек-еен ( LVI) окисляется стереоселективно и дает единственную 1а 2а - окись ( LVII) как при действии надбензойной кислоты, так и реагента ГПТА-Мо ( СО) в. Структура ее подтверждается восстановлением LiAlH4 в смесь вторичных спиртов LVIII, LIX. Стереонаправленность окисления объяснена [195] согласованным экранирующим действием двух заместителей ( см. стр. [35]
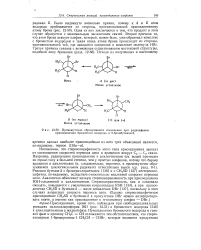 |
Промежуточно образующиеся соединения при радикальном присоединении бромистого водорода к 2-бромбутенам - 2. [36] |
Несомненно, что стереоспецифичность этого типа присоединения зависит от соотношения скоростей переноса цепи и вращения вокруг С2 - С3 связи. Например, радикальное присоединение к циклогексенам ( см. выше) протекает по транс-типу в большей степени, чем у простых олефинов, потому что барьер вращения в циклогексане ( и, следовательно, вероятно, в промежуточно образующемся циклогексильном радикале) относительно высок ( ср. Реакция бутенов-2 с бромтрихлорметаном [ 1361 и с CH3SD [137] нестереоспе-цифична, по-видимому, вследствие относительно медленной скорости переноса цепи. Аналогично объясняют низкую стереонаправленность при присоединении RSH-соединений к циклогексенам. Стереонаправленность, как и следовало ожидать, повышается с увеличением концентрации RSH [133], а при присоединении CH3SD к бутенам-2 - после добавления DBr [137], поскольку в этих случаях возрастает скорость переноса цепи. [37]
Реакция позволяет вводить двойную связь в строго определенное положение с одновременным удлинением углеродной цепи на звено желаемого строения. Однако при реакции Виттига в классическом ее виде обычно образуется смесь стереоизомерных олефинов с преобладанием транс-формы. Выяснено, что на стереонаправленность реакции существенное влияние оказывает растворитель. Так, при осуществлении реакции в диметилформамиде или диметилсульфоксиде на холоду соотношение изомеров резко сдвигается в сторону г ыс-формы. [38]
Несомненно, что стереоспецифичность этого типа присоединения зависит от соотношения скоростей переноса цепи и вращения вокруг С2 - С3 связи. Например, радикальное присоединение к циклогексенам ( см. выше) протекает по транс-типу в большей степени, чем у простых олефинов, потому что барьер вращения в циклогексане ( и, следовательно, вероятно, в промежуточно образующемся циклогексильном радикале) относительно высок ( ср. Реакция бутенов-2 с бромтрихлорметаном [ 1361 и с CH3SD [137] нестереоспе-цифична, по-видимому, вследствие относительно медленной скорости переноса цепи. Аналогично объясняют низкую стереонаправленность при присоединении RSH-соединений к циклогексенам. Стереонаправленность, как и следовало ожидать, повышается с увеличением концентрации RSH [133], а при присоединении CH3SD к бутенам-2 - после добавления DBr [137], поскольку в этих случаях возрастает скорость переноса цепи. [39]
Метод Хильберта - Джонсона [1] является классическим методом получения пиримидиновых нуклеозидов. Он включает конденсацию ди-алкоксипиримидина ( чаще, всего используют диэтокси - или диметокси-производные) с ацилированным гликозилгалогенидом, которая после удаления защитных групп приводит к незамещенному пиримидиновому нуклеозиду. Если гликозилирующим агентом служит более реакционно-способный ацилированный 2-дезоксигликозилгалогенид [2 - 9], метод дает превосходные результаты. Несомненно, что для синтеза дезокси-нуклеозидов метод Хильберта - Джонсона следует предпочесть другим, поскольку в нем отсутствуют щелочные условия, в которых названные дезоксигликозилгалогениды отщепляют элементы галогеноводорода. В большинстве случаев реакция с участием производных 2-дезокси - D-гексоз протекает с высокой стереонаправленностью. Конденсация легко проходит при комнатной температуре, приводя с хорошим выходом почти исключительно к р-аномерам. [40]
Страницы: 1 2 3