Стереохимия - продукт
Cтраница 3
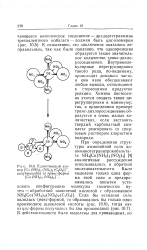 |
Единственный изомер [ Со ( NH3 2 ( N02 2 ( С204 ], получающийся из транс-формы [ Со ( NH3 2 ( Ж 2 4Г. [31] |
Внутримолекулярные перегруппировки такого рода, по-видимому, происходят довольно часто, и они явно обесценивают любые выводы, относящиеся к стереохимии продуктов реакции. Химики постепенно учатся сводить такие перегруппировки к минимуму; так, в приведенном примере гранс-дихлоросоединение образуется в очень малых количествах, если заставить твердый карбонатный комплекс реагировать со спиртовым раствором хлористого водорода. [32]
Этот случай уже представляет большие трудности: помимо построения необходимого углеродного скелета и введения гидроксильной группы, нам предстоит рассмотреть стереохимию заданного продукта. Сначала изобразим его в клиновидной проекции. [33]
Если время существования промежуточного карбаниона достаточно велико и в его молекуле может произойти вращение, то нельзя ожидать соответствия между стереохимией продукта эпоксидации и стереохимией исходного вещества. [34]
Данный обзор преследует цель сопоставить имеющиеся в литературе данные о влиянии стереохимических факторов на кинетику и механизм электродных реакций органических соединений и о стереохимии продуктов электродных реакций, оставляя, однако, в стороне многочисленные данные о стерических препятствиях и нарушении копланарности молекул, вызываемых заместителями. К настоящему времени опубликовано значительное количество оригинальных работ, полностью или частично посвященных указанным в начале вопросам, а последняя попытка обобщения материала о влиянии стереохимических факторов на полярографическое поведение органических веществ была сделана довольно давно [1]; сведения о стереохимии продуктов электрохимических реакций вообще не систематизировались. [35]
Для окончательного решения, по какому механизму протекает реакция замещения, нельзя ограничиваться только кинетическим исследованием реакции, а необходимо привлекать дополнительные сведения о стереохимии продуктов, о влиянии заместителей и растворителей, изотопических эффектах, поведении меченых атомов. [36]
При изучении реакции цинкорганических соединений с солями арилдиазония, приводящей к синтезу с высокими выходами соответствующих арилазосоединений69 - 70, Кэртин нашел, что добавки ди-фенилртути влияют на стереохимию продукта, образующегося из R2Zn, хотя сама она не реагирует с борфторидом фенилдиазония. С увеличением содержания дифенилртути возрастает ( до 80 %) выход менее стабильного г ис-азобензола. Авторы высказали предположение, что здесь играют роль комплексообразующие свойства дифенилртути. [37]
Впервые дается полный обзор литературных данных о кинетике и механизме электродных реакций с участием геометрических изомеров соединений с кратными связями, цис и транс-изомеров алициклического ряда и диастереоизомеров, а также о стереохимии продуктов электроокисления и электровосстановления органических соединений. [38]
Стерическое направление ферментативных реакций, протекающих стереоспецифично, начиная от исходных веществ и кончая оптически чистыми хиральными продуктами, также можно объяснить с помощью аналогичных представлений, поскольку трехмерная структура комплекса фермент - субстрат задает определенное направление, по которому реагент атакует адсорбированную молекулу и, следовательно, определяет абсолютную стереохимию продукта. В качестве примера можно привести стереоспецифическое восстановление пировиноградной кислоты до L-МОЛОЧНОЙ кислоты, катализируемое лактатдегидрогеназой. [39]
Константа скорости бимолекулярной реакции [ базирующаяся на общей ( свободной и связанной в комплекс) концентрации реагирующих веществ ] диена ( например, 9, 10-диметилантрацена) с малеиновым ангидридом уменьшается по мере того, как концентрация диенофила в среде возрастает. Стереохимия продуктов предсказывается в общем правильно, если предположить, что присоединение происходит предпочтительно тогда, когда оба реагирующих вещества ориентированы таким образом, что достигается максимальное перекрывание их ненасыщенных центров. [40]
В) происходит двухэлектронное окисление. Стереохимия продуктов не определялась, а выходы не сообщаются. [41]
Тогда значительно более высокую скорость сольволиза изомера 43 должно обусловливать анхимерное содействие. Стереохимию продукта также можно объяснить участием в качестве интерме-диата иона 47, так как в этом неклассическом ионе положения 1 и 2 эквивалентны и атака нуклеофила по этим положениям должна происходить с одинаковой легкостью, но по э / сзо-направ-лению в каждом случае. [42]
Окисление смеси изопрен - ацетат привело к образованию 3-метилгексена и высших углеводородов. О стереохимии продуктов упомянуто не было. Трифторапетат и бутадиен дали смесь, которая содержала 1 1 1 10 10 10-гексафтор - 3 7-декадиен. Такого типа эксперимент был проведен также с двухосновными кислотами, которые не образуют димеров Кольбе. [43]
Бордуэл и Лэндис [50] получили металлоорганические производные действием на цис - и транс-2 - бромбутены-2 лития в эфире или бутиллития и затем ввели их в реакцию электрофильного замещения с / г-толилдисульфидом. Судя по стереохимии продуктов реакции, обе стадии ( образование и превращение металлоорганического производного) протекают на 75 - 85 % с сохранением конфигурации винильного углерода независимо от способа получения литиевого производного. [44]
Молекула брома координируется по двойной связи алкена, дальнейшее перераспределение электронов приводит к образованию продукта реакции. На основании стереохимии продуктов можно показать, что для большинства олефинов этот механизм неверен. [45]
Страницы: 1 2 3 4