Простое столкновение
Cтраница 2
Значит, в 81 раз слабее притягиваются ионы, и простого столкновения становится достаточно для электролитической диссоциации - распада молекул на ионы при растворении. Количество свободных зарядов - ионов - резко возрастает. [16]
Значит, в 81 раз слабее притягиваются ионы, и простого столкновения становится достаточно для электролитической диссоциации - распада молекул на ионы при растворении. Количество свободных зарядов - ионов - резко возрастает. [17]
Поступательные степени свободы имеют наименьшее время релаксации, так как даже простые столкновения между молекулами приводят к существенному изменению поступательного движения молекул. Таким образом, резкое изменение энергии поступательного движения возможно на длине порядка длины свободного пробега молекулы. [18]
Согласно этой теории процесс сгорания начинается и развивается не в результате простого столкновения и взаимодействия молекул реагирующих веществ, а вследствие соударения в начале только некоторых молекул кислорода, которые в силу ряда физических явлений, предшествующих и сопутствующих сгоранию, становятся более активными, с активными молекулами углеводородов, которые становятся более активными при нагревании. В результате такого столкновения, например одной активной молекулы кислорода с молекулой углеводорода, наряду с нормально начавшимся процессом окисления, возникают новые активные центры, дающие возможность начаться еще одной или нескольким реакциям, которые, в свою очередь, продолжаясь как нормальные реакции окисления, образуют несколько новых активных центров. Так, в упрощенном виде следует понимать разветвление реакций, каждый следующий этап которой является звеном общей цепи реакций. [19]
Реакционный комплекс иногда называют комплексом столкновения, однако совершенно очевидно, что простого столкновения далеко недостаточно для образования структуры, в которой возможен перенос протона. Работа Wr, которую необходимо затратить для образования реакционного комплекса, представляет собой по существу ту часть AF HA, которая не зависит от изменений р / СанА - Величина Wr, необходимая для переноса протона с членов гомологического ряда кислородных кислот на один и тот же субстрат, согласно предположению, определяется потерями энтропии при фиксации молекулы кислоты и свободной энергией ее десольватации. Свободная энергия десольватации третичных аминов практически не коррелирует с их основностью. Сольватация аминов обусловлена главным образом ван-дерваальсовскими взаимодействиями, которые играют заметную роль и при сольватации ионов, поэтому разумно предположить, что свободная энергия десольватации аммониевых солей также никак не связана с их кислотными свойствами. Было показано, что даже прочность водородных связей лишь слабо коррелирует с силой кислот. [20]
Более того, столкновения с четко определенной относительной ориентацией соответствуют даже большему уменьшению энтропии, чем простые столкновения, и, таким образом, энтропия активации должна быть более отрицательной и соответствовать значению Р меньше единицы. Поэтому энтропия активации соответствует как частоте столкновений Z, так и стерическому фактору Р в простой теории столкновений. [21]
Более того, столкновения с нетко опрел елейной относительной ориентацией соответствуют даже большему уменьшению энтропии, чем простые столкновения, и, таким образом, энтропия активации должна быть более отрицательной и соответствовать значению Р меньше единицы. Поэтому энтропия активации соответствует как частоте столкновений Z, так и стерическому фактору Р в простой теории столкновений. [22]
Более того, столкновения с нетко пред елейной относительной ориентацией соответствуют даже эльшему уменьшению энтропии, чем простые столкновения, и, аким образом, энтропия активации должна быть более отрица-йльной и соответствовать значению Р меньше единицы. Поэтому нтропия активации соответствует как частоте столкновений Z, ак и стерическому фактору Р в простой теории столкновений. [23]
Однако не нужно даже производить никаких вычислений, чтобы представить себе, насколько маловероятен такой вариант по сравнению с только что описанной последовательностью простых столкновений. Таким образом, вероятность этой последней настолько больше, чем у всякой другой возможной схемы превращений, что все остальные варианты можно просто не принимать в расчет как не характерные для рассматриваемой газовоздушной смеси. [24]
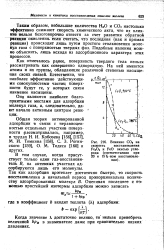 |
Влияние COj на скорость восстановления Fe3O4 и FeO окисью углерода ( соответственно при 20 и 15 % - ном восстановлении. [25] |
Таким образом, небольшие количества Н2О и СО2 настолько эффективно снижают скорость химического акта, что их влия-вие нельзя безоговорочно отнести за счет развития обратной Т акщга окисления, если Г считать, что последняя ( как и прямая реакция) происходит лишь путем простого столкновения молекул газа с поверхностью твердых фаз. [26]
Это уравнение ( как и другие данные) указывает на простоту механизма. Реакция происходит при простом столкновении молекулы водорода и молекулы иода с одновременным образованием двух молекул йодистого водорода. [28]
Имеется еще очень мало доказательств за или против такого приближения. С точки зрения теории простых столкновений это приближение вполне приемлемо - оно не вносит значительной ошибки в расчет стационарных концентраций. [29]
Имеется еще очень мало доказательств за или против такого приближения. С точки зрения теории простых столкновений это приближение вполне приемлемо - оно не вносит значительной ошибки в расчет стационарных концентраций. [30]
Страницы: 1 2 3 4
