Простое столкновение
Cтраница 4
Предположим, что п тел, рассматриваемых как точки, движутся по законам ньютоновского тяготения. В самом деле, в то время как простые столкновения являются нормальным явлением для закона обратных кубов, кратные столкновения, несомненно, бесконечно редки при любом законе. [46]
Уже одно это показывает, что увеличение скорости реакции с температурой нельзя объяснить только через увеличение числа соударений молекул. Но в действительности скорость реакции оказывается гораздо меньше рассчитанной величины. Отсюда следует вывод, что для акта химического взаимодействия недостаточно простого столкновения молекул. Мы знаем, что каждая молекула представляет собой облако отрицательного заряда, окружающее положительно заряженные ядра. При столкновении молекул эти облака должны отталкиваться друг от друга. [47]
 |
Схематическое изображение эксперимента Резерфорда. [48] |
Эти заметные отклонения небольшой части а-частиц были объяснены следующим образом: так как большинство а-частиц проходило сквозь фольгу без отклонений, то в ней, следовательно, ничто не препятствовало их прохождению. Следовательно, это свободное пространство должно быть в самих атомах. Наблюдавшиеся углы отклонения а-частиц были слишком велики, чтобы их можно было объяснить простыми столкновениями. Поэтому для того, чтобы произошло отталкивание в соответствии с законом Кулона ( рис. 5.2), положительно заряженные частицы должны проходить вблизи заряда того же знака. Из соотношения чисел отклонившихся и не отклонившихся частиц Резерфорд вычислил, что положительное ядро занимает очень небольшой объем в центре атома ( см. далее, разд. [49]
Для замещения в ионите многозарядного иона на несколько однозарядных должно произойти одновременное сближение нескольких однозарядных ионов с ионогенными группами ионита, связанными с многозарядными ионами. С разбавлением раствора увеличивается вероятность поглощения многозарядных ионов ионитом, так как вероятность сложных столкновений уменьшается быстрее вероятности простых столкновений. [50]
Следует однако предостеречь от слишком упрощенного применения закона действия масс к гетерогенным реакциям с участием твердых тел. На твердых поверхностях происходят адсорбционные явления, и если реакция идет около этих поверхностей: ( как это имеет место в большинстве гетерогенных каталитических процессов), то скорость ее определяется концентрацией: на поверхности или около нее; последняя часто значительно разнится от концентрации в объеме. Следует также иметь в виду, 1то далеко не всегда ( особенно в тех же гетерогенных реак-диях) механизм реакции сводится к простым столкновениям меж-цу реагирующими молекулами. [51]
В этой главе рассматривается поступательное движение сово-1 купности атомов и молекул в газообразном состоянии и выясняется, как можно объяснить свойства газов на основе ] 1остоянпого поступательного движения частиц, составляющих эту совокупность. Пол -, ная проблема, учитывающая движение молекул под влиянием их взаимодействия Друг с другом, рассматривается динамической теорией; некоторые ее аспекты ( простые столкновения атомов) были затронуты в гл. [52]
Рассмотренная выше реакция ( так же, как и любая другая) имеет еще один чрезвычайно важный аспект. Обратим, например, внимание на стадию отрыва атома водорода от молекулы метана атомом хлора. Выше уже отмечалось, что эта стадия экзотермична на 1 ккал и что фактор ориентации вряд ли действует в этом случае особенно жестко. Тем не менее простого столкновения между реагентами, в том числе и должным образом ориентированного, в общем случае недостаточно для того, чтобы послужить причиной реакции. Можно принять, что на вершине барьера водород связан частично с хлором, частично с углеродом. [53]
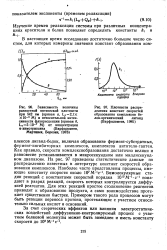
Как правило, скорости комплексообразования достаточно велики и равновесие устанавливается в микросекундном или миллисекунд-ном диапазоне. На рис. 97 приведены статистические данные по распределению известных в литературе констант скоростей образования комплексов. Бимолекулярные стадии реакций с константами скоростей порядка 1010М - 1-с 1 попадают в разряд реакций, скорость которых контролируется диффузией реагентов. Для этих реакций простое столкновение реагентов приводит к образованию продукта, а само взаимодействие протекает существенно быстрее. Примером такого рода процессов могут быть реакции переноса протона, протекающие с участием относительно сильных кислот и оснований. [55]
В этой главе рассматривается поступательное движение сово-i купности атомов и молекул в газообразном состоянии и выясняет -, ся, как можно объяснить свойства газов на основе достоянного поступательного движения частиц, составляющих эту совокупность. Это означает, что мы будем изучать кинетическую теорию газов. Пол-1 ная проблема, учитывающая движение молекул под влиянием их взаимодействия Друг с другом, рассматривается динамической теорией; некоторые ее аспекты ( простые столкновения атомов) были затронуты в гл. [56]
В этой главе рассматривается поступательное движение сово-1 купности атомов и молекул в газообразном состоянии и выясняет -, ся, как можно объяснить свойства газов на основе достоянного поступательного движения частиц, составляющих эту совокупность. Эга означает, что мы будем изучать кинетическую теорию газов. Пол -: ная проблема, учитывающая движение молекул под влиянием их взаимодействия Друг с другом, рассматривается динамической теорией; некоторые ее аспекты ( простые столкновения атомов) были затронуты в гл. [57]
Было высказано предположение, что реакция протекает по гарпунному механизму. Вместо двух нейтральных частиц теперь образуются два иона, между которыми имеется кулоновское притяжение: это веревка гарпуна. Под ее влиянием ноны начинают двигаться вместе ( между ними находится веревка), начинается реакция, появляются КВг Br, Гарпун расширяет сечение реакционного столкновения, и, взяв о как среднее из значений для простых столкновений К К и Вгг Вг2, мы занижаем скорость реакции. [58]
Страницы: 1 2 3 4