Строение - атом - элемент
Cтраница 1
 |
Схемы строения атомов элементов, имеющих заряд ядра. [1] |
Строение атомов элементов принято изображать схематически: электронные слои - в виде концентрических окружностей, электроны - маленькими кружками, а ядро в центре схемы атома - точкой. [2]
Строение атомов элементов принято изображать схематически. На схеме, дающей представление о послойном распределении электронов, электронные слои изображают в виде концентрических окружностей. Электроны, заполняющие слои, представлены маленькими кружками. Ядро изображают в центре схемы атома точкой. [3]
Строение атомов элементов главной подгруппы IV группы полностью соответствует друг другу. Но, как в третьей группе периодической системы, элементы, стоящие в побочной подгруппе ( скандий, иттрий, лантан и актиний), несмотря на то что строение их атомов отличается от строения атома алюминия, в некоторых отношениях больше похожи на алюминий, чем его более тяжелые аналоги, стоящие в главной подгруппе, строение атомов которых соответствует строению атома алюминия; так и элементы четвертой группы, стоящие в побочной подгруппе ( титан, цирконий, гафний и торий), в некоторых отношениях более похожи на кремний, чем его аналоги из четвертой главной подгруппы. Однако только последние, подобно углероду и кремнию, проявляют четырехвалентность по отношению как к электроположительным, так и к электроотрицательным веществам и образуют с водородом легколетучие соединения. Эта способность особенно характерна для важнейшего представителя главной подгруппы IV группы - углерода. [4]
Строение атомов элементов главной подгруппы IV группы полностью соответствует друг другу. Но, как в третьей группе периодической системы, элементы, стоящие в побочной подгруппе ( скандий, иттрий, лантан и актиний), несмотря на то что строение их атомов отличается от строения атома алюминия, в некоторых отношениях больше похожи на алюминий, чем его более тяжелые аналоги, стоящие в главной подгруппе, строение атомов которых соответствует строению атома алюминия; так и элементы четвертой группы, стоящие в побочной подгруппе ( титан, цирконий, гафний и торий), в некоторых отношениях более похожи на кремний, чем его аналоги из четвертой главной подгруппы. Однако только последние, подобно углероду и кремнию, проявляют четырехвалентность по отношению как к электроположительным, так и к электроотрицательным веществам и образуют с водородом легколетучие соединения. Эта способность особенно характерна для важнейшего представителя главной подгруппы IV группы - углерода. У кремния она проявляется не в такой мере вследствие его склонности к образованию кислородных соединений, в первую очередь определяющей поведение кремния. Тот факт, что в определенных классах соединений проявляется особенно большое сходство между кремнием и элементами побочной подгруппы, соответствует правилу, которое постоянно отмечалось в предыдущих группах: второй элемент главной подгруппы является переходным к элементам побочной подгруппы. [5]
Рассмотрим строение атомов элементов в последовательности возрастания их порядковых номеров. [6]
Для строения атомов электронно-избыточных элементов, расположенных в конце периодов в периодической системе, характерно наличие пар электронов на валентных АО. Спаривание электронов снижает валентные возможности атомов. [7]
 |
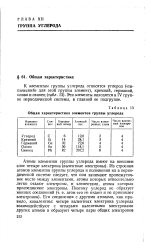
Общая характеристика элементов группы углерода. [8] |
Из строения атомов элементов группы углерода и положения их в периодической системе следует, что они занимают промежуточное место между элементами, атомы которых относительно легко отдают электроны, и элементами, атомы которых присоединяют электроны. [9]
Рассмотрим строение атомов элементов малых периодов и установим, какая связь существует между строением атома и периодической системой элементов. [10]
 |
Общая характеристика элементов группы углерода. [11] |
Из строения атомов элементов группы углерода и положения их в периодической системе следует, что они занимают промежуточное место между элементами, атомы которых относительно легко отдают электроны, и элементами, атомы которых присоединяют электроны. [12]
 |
Общая характеристика элементов группы углерода. [13] |
Из строения атомов элементов группы углерода и положения их в периодической системе следует, что они занимают промежуточное место между элементами, атомы которых относительно легко отдают электроны, и элементами, атомы которых присоединяют электроны. [14]
Объясняется это строением атомов элементов. У атома натрия на внешнем энергетическом уровне находится один электрон, отдав который, атом превращается в ион с 8 электронами на внешнем уровне, как у атома инертного газа неона. Атом хлора содержит на внешнем уровне 7 электронов. Приняв один электрон, он переходит в ион с устойчивым электронным уровнем, как у атома инертного газа аргона. [15]
Страницы: 1 2 3 4