Строение - молекула - вода
Cтраница 2
Диссоциация кислот, оснований и солей в водной среде объясняется строением этих веществ и дипольным строением молекул воды. Как известно, в молекулах воды положительные и отрицательные заряды распределены неравномерно и расположены в противоположных концах молекулы. Ионные соединения состоят из противоположно заряженных ионов. Сила взаимного притяжения, действующая между противоположно заряженными нонами электролита, находящегося в воздушной среде, ослабевает в воде настолько, что это приводит к полной или частичной диссоциации электролита на самостоятельные ионы. [16]
Диссоциация кислот, оснований и солей в водной среде объясняется строением этих веществ и дипольным строением молекул воды. Как известно, в молекулах воды положительные и отрицательные заряды распределены неравномерно и расположены в противоположных концах молекулы. Ионные соединения состоят из противоположно заряженных ионов. [17]
Диссоциация кислот, оснований и солей в водной среде обусловлена ионным строением этих веществ и строением молекул воды. [18]
В первой главе дан анализ отечественной и зарубежной научно-технической литературы по физике и химии воды, описывающие строение молекул воды и их ассоциацию. [19]
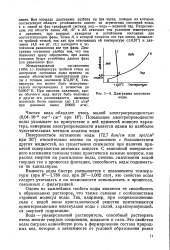 |
Диаграмма состояния воды. [20] |
Одним из важнейших свойств воды является ее способность к образованию растворов, что также связано с особенностями строения молекул воды. Так, например, при соприкосновении соли с водой ионы кристаллической решетки притягиваются ориентированными молекулами воды с силой, характеризующей, ся энергией гидратации. [21]
 |
Диаграмма состояния воды. [22] |
Одним из важнейших свойств воды является ее способность к образованию растворов, что также связано с особенностями строения молекул воды. Так, например, при соприкосновении соли с водой ионы кристаллической решетки притягиваются ориентированными молекулами воды с силой, характеризующейся энергией гидратации. [23]
В настоящее время разделение по Ланге и К. П. Мищенко является общепринятым, несмотря на эволюцию наших представлений о строении молекулы воды. В пользу такого разделения для водных растворов говорит множество опытных данных, и нет пока ни одного экспериментального факта, отвергающего его. [24]
В настоящее время разделение по Ланге и К. П. Мищенко является общепринятым, несмотря на эволюцию наших представлений о строении молекулы воды. В пользу такого разделения для водных растворов говорит множество опытных данных. [25]
Предложенные до настоящего времени модельные методы расчета ( некоторые из них рассматриваются ниже) используют либо различные представления о строении молекул воды, либо исходят из различных представлений о воде, как о жидкой фазе. [26]
 |
Относительная прочность и угловое распределение связывающих орбиталей. [27] |
Строение молекул воды, аммиака и аналогичных им соединений было уже рассмотрено в предположении, что образуется чистая р-связь. [28]
Такое строение молекул воды определяет и характер образуемых ими связей. Так как эти связи осуществляются протонами, они получили название водородных. Каждая молекула может давать четыре водородные связи. [29]
Таким образом, электричество переносится не только мигрирующими ионами Н3О, но и протонами, переходящими от одной молекулы воды к другой. На основании данных о строении молекул воды было подсчитано, что от иона НзО к молекуле воды протон проходит расстояние 0 86 10 - 8 см, что соответствует перемещению Н3О в электрическом поле на 3 1 10 - 8 см. При таком механизме подвижность НзО оказывается значительно больше по сравнению с тем, когда этот ион перемещается только миграцией. Из схемы ( а) видно, что молекулы воды в левой и правой ее частях имеют различную ориентацию. Для обеспечения непрерывного перехода протона от НзО к Н2О необходимым условием является изменение ориентации молекулы ( 2), от которой ушел протон. Она должна занять положение, соответствующее молекуле ( 1), для того, чтобы принять новый протон, движущийся в том же направлении. Аналогичным образом объясняется повышенная подвижность иона гидроксила. [30]
Страницы: 1 2 3 4