Влияние - ионная атмосфера
Cтраница 1
Влияние ионной атмосферы характеризуется некоторой функцией от концентрации; эта функция называется активностью ионов. [1]
 |
Ионная оболочка вокруг катиона ( а и со - а С. [2] |
Влияние ионной атмосферы сказывается не только на электропроводности, но и на скоростях реакций с участием ионов, что приводит к непостоянству констант равновесия. [3]
Влияние ионной атмосферы характеризуется некоторой функцией от концентрации; эта функция называется активностью ионов. [4]
 |
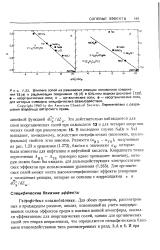
Вальденовские произведения м ( Ом - ] см2 моль 1 сП различных ионов в разных растворителях ( при нулевой ионной силе, Т 298 К. [5] |
Влияние ионной атмосферы на миграцию иона во внешнем поле проявляется за счет двух эффектов - релаксационного и электрофоретического. [6]
Так как поведение иона обусловлено влиянием ионной атмосферы, рассматриваются все ионы, присутствующие в растворе. [7]
 |
Зависимость удельной. [8] |
Подвижности ионов при увеличении концентрации раствора уменьшаются вследствие возрастающего влияния ионной атмосферы. [9]
Это выражение является необычным, поскольку в нем не отражено влияние ионной атмосферы и обычном смысле. Члены ф и V относятся к настолько плотно упакованной системе ионов, что их распределение, невидимому, подобно распределению ионов в кристаллической решетке, а фу соответствует исчезновению ионной атмосферы при бесконечном удалении ионов друг от друга. Два следствия из этого эмпирического уравнения представляют значительный интерес. Во-первых, из табл. 49 и 50 следует, что как fy, так и ср являются аддитивными величинами. Однако к отмеченному Рутом и другими исследователями свойству приблизительной аддитивности S-у следует относиться с осторожностью, так как в уравнение ( 77) входит величина ф, которая может значительно меняться при переходе от одной кристаллической структуры к другой. В этом случае величина Sv не является аддитивной. [10]
Это выражение является необычным, поскольку в нем не отражено влияние ионной атмосферы в обычном смысле. Члены ф и V относятся к настолько плотно упакованной системе ионов, что их распределение, повидимому, подобно распределению ионов в кристаллической решетке, а - ] соответствует исчезновению ионной атмосферы при бесконечном удалении ионов друг от друга. Два следствия из этого эмпирического уравнения представляют значительный интерес. Во-первых, из табл. 49 и 50 следует, что как Фу, так и ср являются аддитивными величинами. Однако к отмеченному Рутом и другими исследователями свойству приблизительной аддитивности Sv следует относиться с осторожностью, так как в уравнение ( 77) входит величина ], которая может значительно меняться при переходе от одной кристаллической структуры к другой. В этом случае величина Sy не является аддитивной. [11]
Смысл члена g ( с) состоит в том, что он отражает влияние ионных атмосфер в выражении закона действующих масс и их влияние на электропроводность. [12]
Формула ( 48) пригодна только для разбавленных растворов, так как при ее выводе влиянием ионной атмосферы пренебрегали. Поэтому существуют теоретические основания ожидать изменения величины kD с изменением ионной силы. [13]
Таким образом, наблюдаемое замедление реакции в разбавленных растворах, возможно, определяется, как и предполагалось, влиянием ионной атмосферы. Однако специфические взаимодействия с катионами щелочных металлов также приводят к замедлению процесса, поскольку в этаноле кинетику декарбоксилирования можно объяснить, считая реакционноспособными только свободные ионы и приняв нулевыми константы скорости для ионных пар. [14]
Страницы: 1 2 3