Влияние - лиганд
Cтраница 2
Основным эффектом влияния лигандов, как и в случае электронной конфигурации из одного d - электрона, остается расщепление термов. Но в отличие от случая dl для нескольких cf - электронов наглядная интерпретация затруднительна. [16]
В результате влияния лигандов наблюдается упрочнение связей М - СО в M ( CO) ML по сравнению с М ( СО) п 1, причем транссвязи М - СО будут упрочняться сильнее, чем цис-связи. [17]
Для выяснения влияния различных лигандов, т.е. природы хелатного узла, были изучены аквокомплексы кобальта, а также его комплексы с рядом азотсодержащих органических лигандов. [18]
 |
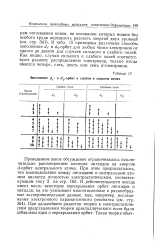
Константы кислотной диссоциации комплексов платины ( II ( при 25 С. [19] |
Это свидетельствует о направленном влиянии я-акцепторных лигандов на кислотные свойства внутрисферных молекул воды. Замена же диметилсульфоксида в 1Р1 ( г4Н3) 2 ( ДМСО) Н2О ] 2 1 на аммиак, как и следует ожидать, приводит к резкому уменьшению константы диссоциации. [20]
С точки зрения учета влияния лигандов на электронную конфигурацию центрального иона описанная модель комплексного иона отвечает внутримолекулярному эффекту Штарка, причем ион металла считается помещенным в электростатическое поле лигандов, которые предполагаются фиксированными и неполяризуемыми. Удобно считать, что ядро центрального иона находится в начале системы координат. Допустим, что расположение лигандов обладает определенной симметрией, отвечающей точечной группе G. Такую же симметрию имеет потенциал поля лигандов ( см. разд. [21]
Подобное расщепление определяется суммой влияния лигандов, расположенных на каждой из координат. [22]
Вместо того чтобы пытаться делить влияние лигандов на отдельные составные части, предположим, что их результирующая может быть описана определенной простой моделью. [23]
Образование транс-нитрила при карбонилировании объясняется влиянием лигандов промежуточного пятикоординационного комплекса, предположение о существовании которого было уже высказано выше. Поведение акрилонитрильного лиганда в реакции сдваивания ( 20) довольно неожиданно, так как при тех же условиях замена нитрильной группы на другую электронооттяги-вающую группу, например карбометоксигруппу, приводит к образованию смеси цис - и гранс-эфиров с преобладанием транс-компоненты. В литературе имеется по меньшей мере одно сообщение о получении комплекса типа XIII [59], в котором алкилаллильная группа обладает ангм-конфигурацией, чго. [24]
 |
Заполнение d - и - орбит в слабом и сильном полях. [25] |
Проведенное выше обсуждение ограничивалось исключительно рассмотрением влияния лигандов на энергии rf - орбит центрального атома. При этом предполагалось, что взаимодействие между лигандами и центральным атомом является полностью электростатическим, соответствующим типу 2 на стр. В действительности всегда имеет место некоторое перекрывание орбит лигандов и металла; на это указывают многочисленные и разнообразные экспериментальные данные, как, например, исследования электронного парамагнитного резонанса ( см. стр. При дальнейшем развитии теории к электростатическим представлениям теории кристаллического поля были добавлены идеи о перекрывании орбит. [26]
Уже в первых работах по изучению влияния лигандов на активность катализатора Си в реакции гидролиза DFP [30] было замечено, что наилучшими активаторами являются такие энергичные акцепторы электронов, как дипиридил, трипиридил, фенантролин и их производные. Кроме того, активирующ им действием обладают и другие амины, которые в условиях реакции образуют с катализатором не очень прочные комплексы и удерживают его в растворе. [27]
 |
Комплексы d5 слабого и сильного полей. [28] |
Когда d - орбитали расщепляются под влиянием лигандов, средняя энергия после расщепления должна быть равной энергии в сферическом поле до расщепления. [29]
Очевидно, требуются большие систематические исследования по влиянию лигандов на каталитическую активность систем с соединениями переходных металлов. [30]
Страницы: 1 2 3 4