Влияние - неоднородность - поверхность
Cтраница 2
Однако само по себе спрямление экспериментальной изотермы в координатах p / V и р еще недостаточно для суждения о применимости теории Лэнгмюра, так как влияние неоднородности поверхности ( неравноценность адсорбционных центров, непостоянство взаимодействий адсорбат-адсорбент) и влияние взаимодействий адсорбат-адсорбат, компенсируя друг друга, могут привести к чисто формальному описанию опыта уравнением Лэнгмюра. [16]
Измерения теплоты адсорбции на неорганических кристаллических веществах менее пригодны для данной цели. В рассмотренных случаях влияние неоднородности поверхности настолько сильно, что снижение теплоты адсорбции с увеличением покрытия проявляется очень четко. Дрейн и Моррисон [25] указывали, что хотя qst для аргона, кислорода и особенно азота начинает убывать даже при малых покрытиях, вблизи точки х - хт наблюдается второй спад. [17]
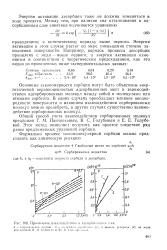 |
Проявление взаимодействия в адсорбционном слое. [18] |
Основные закономерности сорбции могут быть объяснены энергетической неравноценностью адсорбционных мест и взаимодействием адсорбированных молекул между собой и молекулами или атомами сорбента. В одних случаях преобладает влияние неоднородности поверхности и влиянием взаимодействия сорбированных молекул можно пренебречь, в других случаях существенно взаимодействие сорбированных молекул. [19]
Хорошо известно, что лишь немногие адсорбенты обладают однородной поверхностью. Реальные поверхности, как правило, являются гетерогенными Влияние неоднородности поверхности часто превосходит роль межмолекулярных взаимодействий в поверхностной фазе. Поэтому важной проблемой является определение энергетической гетерогенности адсорбентов из экспериментальных изотерм адсорбции. Для описания гетерогенности адсорбентов большинство авторов использует функцию распределения энергии адсорбции F ( U), где U - энергия адсорбции. Функция F ( U) не содержит информации о топографии распределения адсорбционных центров. Она дает только информацию об общей, гетерогенности поверхности адсорбента. [20]
Еще слишком рано говорить о том, будет ли на основе этого нового метода создан общий метод определения удельной поверхности. Достигнутые успехи позволяют надеяться, что этот метод даст возможность учесть одновременно и влияние неоднородности поверхности и межмолекулярное притяжение в адсорбционном слое. Поэтому с интересом следует ожидать дальнейших результатов. Однако следует помнить, что все толкования основаны на постулате о протекании лишь мономолекулярной адсорбции в интересующей нас области изотермы. Это может быть вполне обоснованным, когда чистая теплота адсорбции ( q - L) высока ( резкий подъем изотермы, высокие значения СБЭТ); так, метод применим для области низких относительных давлений. Но при рассмотрении систем с низкой теплотой адсорбции ( постепенный рост адсорбции, изотерма III типа) возникают сомнения в правильности этого постулата. А в тех случаях, когда заметная полимолекулярная адсорбция происходит прежде, чем закончится образование плотного монослоя, модель де Бура - Хилла неприменима. [21]
С другой стороны, физическая адсорбция азота или окиси углерода, или какого-либо другого газа происходит одинаково легко как на молекулах А1203, так и на атомах железа. Этот факт делает невозможным определение части поверхности катализатора, покрытой промотором. Хотя влияние неоднородности поверхности на ван-дер-ваальсову адсорбцию не столь заметно, как на хемосорбцию, им нельзя ни в коей мере пренебрегать. Из предыдущих глав мы видели, что теоретически рассчитанные теплоты адсорбции газа на поверхностях углерода, металла или ионного кристалла не очень различны и что экспериментальные данные подтверждают теорию для менее активной, однородной части поверхности. Однако, несмотря на то, что теплота адсорбции молекул приблизительно одна и та же на гладких поверхностях углерода и железа, существует большое различие в том, испытывает ли молекула притяжение со стороны двух поверхностей углерода или со стороны одной. Другими словами, теплота адсорбции в узких трещинах и щелях резко отличается от теплоты на гладкой поверхности адсорбента. [22]
С другой стороны, физическая адсорбция азота или окиси углерода, или какого-либо другого газа происходит одинаково легко как на молекулах А12О3, так и на атомах железа. Этот факт делает невозможным определение части поверхности катализатора, покрытой промотором. Хотя влияние неоднородности поверхности на ван-дер-ваальсову адсорбцию не столь заметно, как на хемосорбцию, им нельзя ни в коей мере пренебрегать. Из предыдущих глав мы видели, что теоретически рассчитанные теплоты адсорбции газа на поверхностях углерода, металла или ионного кристалла не очень различны и что экспериментальные данные подтверждают теорию для менее активной, однородной части поверхности. Однако, несмотря на то, что теплота адсорбции молекул приблизительно одна и та же на гладких поверхностях углерода и железа, существует большое различие в том, испытывает ли молекула притяжение со стороны двух поверхностей углерода или со стороны одной. Другими словами, теплота адсорбции в узких трещинах и щелях резко отличается от теплоты на гладкой поверхности адсорбента. [23]
В модели Лэнгмюра-БЭТ ( Брюнауэра-Эммета - Теллера) принимается, что адсорбция локализована во всех слоях, причем энтальпия адсорбции в первом слое является некоторой постоянной величиной, а в последующих слоях равна теплоте конденсации, т.е. второй и последующие слои характеризуются свойствами объемной фазы. Здесь явно необходимо знать коэффициент поверхностной диффузии. При этом необходимо учитывать влияние неоднородности поверхности. [24]
 |
Профили изопотенциальных-поверхностей вблизи поверхности адсорбен-та. [25] |
БЭТ, осложняется достаточно широкими возможностями выбора алгебраического вида изотермы и достаточно большим числом подгоночных параметров ( vm, с и k), так что обычно трудно определить, насколько серьезное значение следует придавать тому, что данная изотерма описывает конкретные данные. Проблема возможных фазовых изменений обсуждается в разд. XIV - 11, а влияние неоднородности поверхности - в разд. [26]
С точки зрения физической адсорбции величина удельной поверхности является одной из наиболее важных характеристик адсорбента, но не единственно важной. Неоднородность поверхности играет весьма существенную роль, в частности при адсорбции газов при низких давлениях, как это было установлено в предыдущей главе. Первая часть настоящей главы посвящена обсуждению влияния неоднородности поверхности на ван-дер-ваальсову адсорбцию. Эта часть включает адсорбционные опыты, проведенные на гладких, или обычно считаемых гладкими, поверхностях, что представляет большой теоретический интерес. [27]
Однако сама по себе симметричность пиков при малых пробах, представляя необходимое условие для того, чтобы считать поверхность однородной, еще не является достаточным условием. Это вытекает из того, что при малых пробах адсорбата и высоких температурах колонны, особенно если этот адсорбат на данном адсорбенте адсорбируется не очень сильно, можно практически приблизиться к уравнению Генри для изотермы адсорбции, а следовательно, получить симметричные пики и в случае неоднородной поверхности. Близкая к линейной изотерма адсорбции в области малых заполнений может получиться и благодаря компенсации влияния неоднородности поверхности противоположным влиянием взаимного притяжения адсорбированных молекул. [28]
Условность приведенной классификации связана также и с тем, что на каталитические свойства металлов значительное влияние оказывает способ приготовления катализаторов. По-разному приготовленные катализаторы отличаются друг от друга не только удельной поверхностью, величина которой является экстенсивным фактором изменения каталитической активности, но обладают также различной степенью структурной неоднородности поверхностей. Хотя эта проблема имеет важнее значение для гетерогенного катализа в целом, для металлических катализаторов влияние неоднородности поверхности па каталитические свойства в настоящее время исследовано нрлболее глубоко. [29]
Этот метод мог бы иметь некоторую ценность, если бы он действительно позволял находить энергию взаимодействия адсорбат - адсорбат. К сожалению, однозначное решение этой задачи невозможно. Хорошо известно, что в общем случае по виду изотермы или кривой теплот адсорбции невозможно отличить влияние неоднородности поверхности от проявления сил отталкивания между адсорбированными молекулами. Столь же неоднозначно истолкование полученных экспериментальных данных и при существовании аттракционных взаимодействий между адсорбированными молекулами. Так, например, если часть катионов в полостях цеолита делокализована и эти катионы обладают некоторой свободой перемещения, то рост адсорбции должен вызывать уменьшение их подвижности, вследствие чего энтропия цеолита будет уменьшаться, а теплота адсорбции ( для системы адсорбат - адсорбент) будет увеличиваться с ростом заполнения. Подобно этому любая причина, способная вызвать уменьшение энтропии адсорбента, будет вызывать увеличение теплоты. Таким образом, наблюдаемое увеличение Q с Т при адсорбции на цеолитах совершенно не обязательно означает только проявление аттракционных взаимодействий. [30]
Страницы: 1 2 3