Влияние - валентность
Cтраница 1
 |
Прибор для измерения скоро. [1] |
Влияние валентности ( заряда) иона на электропроводность состоит в том, что, чем выше заряд иона, тем большее количество электричества он переносит с одного электрода на другой. Так, например, каждый двухвалентный анион отдает аноду два электрона, а одновалентный - только один. [2]
Влияние валентности: соли одновалентных металлов образуют е хлористым алюминием большее число комплексных соединений, чем соли многовалентных металлов; нельзя было приготовить комплексные соединения хлористого алюминия с солями четырехвалентных металлов. В подобной же зависимости находится устойчивость комплексных соединений. [3]
Влияние валентности катаионов окислов ванадия на их каталитические свойства в процессе окисления нафталина. [4]
Влияние валентности коагулирующих ионов на порог коагуляции определяется правилом Шульце - Гарди; чем больше валентность коагулирующих ионов, тем больше их коагулирующая сила или тем меньше порог коагуляции. [5]
Влияние валентности коагулирующего иона выражается правилом Шульце-Гарди, которое устанавливает, что коагулирующим ионом при осаждении золен электролитами является ион, заряд которого противоположен заряду коллоидной частицы. Коагулирующее действие такого иона сильно возрастает с ростом валентности иона. [6]
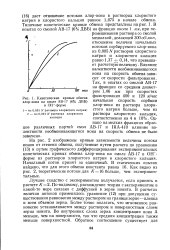 |
Кинетические кривые обмена. [7] |
Влияние валентности необменивающегося иона на скорость обмена зависит от скорости фильтрования. Однако на мелких фракциях образцов различных партий смол АВ-17 и IRA-410 влияние валентности необменивающегося иона на скорость обмена не было замечено. [8]
Рассмотрено влияние валентности, дисперсности распределения и мест локализации Си, Ni, Co, Fe в цеолитном катализаторе на активность последнего в катализе реакций глубокого окисления, гидрирования, гидрокрекинга углеводородов. [9]
Это влияние валентности отчетливо обнаруживается при сопоставлении межатомных расстояний в рядах изоэлектрон-ных соединений. [10]
 |
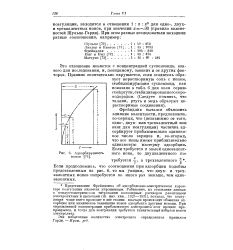
Кривые коагулирующего действия смесей электролитов валентного типа 1 - 2 - 12 ( 7. 1 1 23 - 32 ( 2. [11] |
Рассмотрим теперь влияние валентностей ионов на закономерности коагуляции золей смесями электролитов. Влияние побочных ионов выражается гораздо слабее. Возрастание отношения z / z c их валентностей вызывает небольшое уменьшение положительных и увеличение отрицательных отклонений от аддитивности. Это подтверждается рис. 9 и 10, приведенными в качестве примера. [12]
 |
Адсорбируемость ионов. [13] |
Фрейндлих пытался объяснить влияние валентности, предположив, во-первых, что ( независимо от того, одно -, двух - или трехвалентный ион взят для коагуляции) частичка адсорбирует приблизительно одинаковое число зарядов и, во-вторых, что все ионы имеют приблизительно одинаковую изотерму адсорбции. [14]
На рис. 3 показано влияние валентности. Здесь соответствующие соли двух - и трехвалентного марганца сравниваются в виде ацетатов и ацетилацетонатов. По-видимому, спектры солей марганца с более высокой валентностью также относятся к типу I, но пики расширены и сдвинуты в сторону более высоких энергий. В случае солей трехвалентного марганца основной максимум находится при 25 эв. Этот сдвиг, приписанный изменению валентности, может отражать изменение в электростатическом окружении, укорочение связей и увеличение поляризации ближайших соседних атомов, сопровождающей увеличение валентности. [15]
Страницы: 1 2 3 4