Влияние - валентность
Cтраница 3
Развитые выше представления о катионитах, характеризующие последние как особый класс кислот и солей, особенностями которых являются лишь многовалентность и отсутствие подвижности их анионов и которые не имеют других принципиальных отличий от маловалентных солей и кислот, уже изученных более полно, позволяют в известной мере экстраполировать на систему катионит - растворитель те сведения о влиянии валентности на характер диссоциации электролита, которые получены в результате изучения кислот и солей обычного типа. [31]
Коагуляцию главным образом вызывает один из ионов прибавленного электролита, именно тот, который противоположен по знаку заряду гранул золя. Влияние валентности ионов сказывается очень сильно. [32]
Коагуляцию вызывает главным образом один из ионов прибавленного электролита, а именно тот, который противоположен по знаку заряда гранул золя. Влияние валентности ионов сказывается очень сильно. [33]
В упрощенных уравнениях теории сильных электролитов не учитывается величина радиуса ионов. Грубо ориентировочно влияние валентности ионов на величину коэффициента активности растворенного электролита подтверждается опытными данными. Для растворов электролитов с ионами одинаковой валентности коэффициенты активности обычно имеют близкие величины. Чем выше валентность ионов, тем сильнее отличается раствор сильного электролита от идеального раствора. Однако и для электролитов с одинаковой валентностью ионов различия коэффициентов активности могут достигать значительной величины. Это наблюдается даже у электролитов со сходным строением и сходными химическими свойствами. На этом рисунке показано изменение коэффициента активности в растворах сильных щелочей. [34]
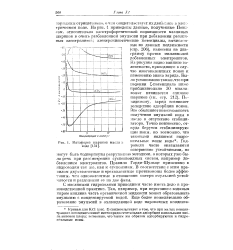 |
Катафорез шариков масла в воде. [35] |
На рис. 1 приведены данные, полученные Повп-сом, относительно электрофоретической подвижности масляных шариков в очень разбавленной эмульсии при добавлении различных электролитов; электрокинетические потенциалы, вычисленные из данных подвижности ( стр. Из рисунка видно влияние валентности, приводящее в случае многовалентных ионов к изменению знака заряда. По-видимому, заряд возникает вследствие адсорбции ионов. Это объясняет невозможность получения эмульсий воды в масле в отсутствие стабилизатора. [36]
Гумусовые вещества коллоидной степени дисперсности представляют собой переходные системы от гидрофобных к гидрофильным. О их гидрофобности свидетельствует относительная легкость коагуляции и влияние валентности коагулирующих ионов на этот процесс. Тем не менее малая чувствительность этих коллоидов к содержанию в воде нейтральных электролитов, значительные количества воды в выпавших осадках гумусовых веществ, проявление защитного действия по отношению к высокодисперсным глинистым и почвенным суспензиям, коллоидной кремнекислоте, золям гидроокиси железа и алюминия свидетельствуют о наличии у гумусовых веществ свойств, присущих гидрофильным коллоидам. [37]
Более подробно материал табл. 9, в том числе влияние валентности металла, будет обсужден дальше, в гл. [38]
Влияние валентности необменивающегося иона на скорость обмена зависит от скорости фильтрования. Однако на мелких фракциях образцов различных партий смол АВ-17 и IRA-410 влияние валентности необменивающегося иона на скорость обмена не было замечено. [39]
Однако использование этого фактора для сближения потенциалов разряда катионов нескольких сортов ( без учета влияния валентности на изменение свободной энергии компонентов, входящих в сплав) не может иметь практического значения, так как возможность выбора электролитов с катионами одного и того же металла различных валентностей достаточно ограничена. [40]
 |
Величины коагулирующей способности. [41] |
Все величины приведенные в табл. 48, вычислены, считая коагулирующую способность одновалентного катиона за единицу. Хотя эти величины, полученные разными исследователями, и расходятся, однако, закономерность влияния валентности ясна. [42]
Определим теперь на оси абсцисс концентрации катионов в растворе - получим отрезки ОЕ, OF и ОК. Легко заметить, что отношение ОЕ: OF: OK гораздо больше отношений 1: 2: 3, что совпадает с только что разобранным влиянием валентности противоположно заряженного иона. [43]
Полученные таким образом теоретические прямые представлены на рис. 49 в виде пунктирных линий. Как видно из рисунка, с приближением к бесконечному разбавлению экспериментальные данные стремятся к значениям, соответствующим предельному закону Дебая - Гюккеля. Влияние валентности на зависимость коэффициента активности от концентрации хорошо согласуется с теорией. Дебая - Гюккеля отражает влияние валентности. [44]
Вторым влияющим на электропроводность фактором является з а-р я д ионов. Очевидно, что при прочих равных условиях большее количество электричества может быть перенесено, например, двухвалентными ионами, чем одновалентными, так как каждый из первых отдает ( или получает) по два электрона. Чтобы устранить влияние валентности ионов, при сравнительном изучении электропроводности пользуются нормальными концентрациями растворов. В этом случае больший заряд иона компенсируется его меньшим содержанием. [45]
Страницы: 1 2 3 4