Влияние - водородная связь
Cтраница 2
Показано также влияние водородных связей на реакционную способность ингибиторов. Например, из сопоставления констант взаимодействия перекисного радикала метилэтилкето на с ингибиторами - а-нафтолом и фенолами различного строения - следует, что эффективность ингибиторов в атом случае значительно меньше, чем в углеводородной среде, что обусловлено образованием водородной связи между кетоном и ингибитором. [16]
Изучая механизм влияния водородных связей на кинети жидкофазных радикальных реакций, Суханова и Бучачен [70] пришли к выводу, что реакции радикалов с сольвати ванными молекулами представляют собой совокупность меньшей мере трех элементарных актов: 1) реакция радика с несольватированной молекулой; 2) реакция с сольвато 3) равновесие сольватации. [17]
Для анализа влияния водородных связей на колебательные частоты пиперидина нами был проведен расчет частот и форм нормальных колебаний фрагмента ассо-циата пиперидина [24], который значительно облегчил интерпретацию спектров. [18]
При рассмотрении влияния водородной связи на электронные спектры молекул необходимо учитывать характер электронного перехода, соответствующего данной полосе спектра, тип водородной связи и особенности структуры молекулы. [19]
Естественно поэтому ожидать влияния водородной связи на реакции окисления углеводородов, в которых образуются такие соединения, как гидроперекиси, спирты, кислоты, способные образовывать водородные связи. [20]
Особенно ярко проявляется влияние водородных связей в тех случаях, когда они приводят к образованию кольцевых структур. [21]
Авторы подробно рассмотрели влияние водородных связей на скорость реакции и ее механизмы. Совокупность экспериментальных данных согласуется с предположением, что обмен протонами происходит в циклическом комплексе, образованном двумя водородными связями. Такая модель призвана объяснить большую скорость реакции и низкую энергию активации. Следует, однако, отметить, что кинетика этих процессов в целом исследована еще недостаточно. Например, оказалось, что константа скорости протонного обмена между НС1 и НВг в результате тщательной очистки системы сильно понизилась, что свидетельствует о наличии неконтролируемых примесей, катализирующих процесс. [22]
Естественно поэтому ожидать влияния водородной связи на реакции окисления углеводородов, в которых образуются такие соединения, как гидроперекиси, спирты, кислоты, способные образовывать водородные связи. [23]
Особенно ярко проявляется влияние водородных связей в тех случаях, когда они приводят к образованию кольцевых структур. [24]
Это различие приписывается влиянию водородной связи между гидроксильной группой и карбонильным атомом кислорода. [25]
Рассмотрены изменения под влиянием водородной связи ВАН BR частоты продольного колебания группы А - Н и протонного химического сдвига в ЯМР, а также некоторые характеристики водородных связей, полученные путем расчетов. [26]
Рассмотрены изменения под влиянием водородной связи RAH - - - BR частоты-продольного колебания группы А - Н и протонного химического сдвига в ЯМР, а также некоторые характеристики водородных связей, полученные путем расчетов. [27]
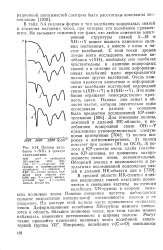 |
Полосы колебания v ( NH в спектре капролактама. [28] |
В средней области ИК-спектра влияние водородных связей отчетливо проявляется в смещении частоты валентного колебания ХН-группы в сторону меньших волновых чисел. Помимо смещения частоты наблюдается сильное возрастание интегральной интенсивности полосы и ее уширение. На контуре этой полосы часто проявляется несколько пиков. Деформационные колебания ХН-группы немного смещаются в область больших волновых чисел, при этом также можно наблюдать изменения интенсивности и ширины полосы. [29]
Морозова, , Данилова В. И. Влияние водородной связи на положение полос поглощения в электронных спектра некоторых замещенных бензола. [30]
Страницы: 1 2 3 4