Влияние - водородная связь
Cтраница 3
Спектральные свойства спиртов и влияние водородных связей на молекулярные спектры мы рассмотрим в конце этой главы. [31]
Это означает, что влияние водородных связей на кривую титрования некооперативной макромолекулы сводится, как это было указано Тэнфордом [22], к изменению константы ионизации. [32]
В данном случае несомненно влияние водородных связей м жду ОН и С02СН3 и между ОН и ОН; последний тип водородной связи более легко осуществляется в оптически активном изомере по сравнению с жезо-формой. [33]
Этот пример также иллюстрирует влияние водородной связи, которая, однако, образована карбонильным, а не эфирным кислородом ацетоксигруппы. [34]
Дан анализ методологии исследований влияния водородных связей на скорость, механизм и направление химических реакций. Подробно рассмотрены про-толитические реакции, проанализирована связь между кислотными и основными свойствами органических соединений и их способностью к образованию водородных связей. Показано существенное влияние среды. [35]
Это также может объясняться влиянием водородной связи [85], но в этом частном случае могут иметь значение и другие факторы. [36]
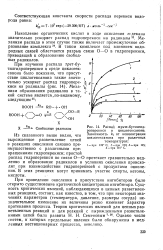 |
Распад трет-бутклгкц-роперекиси в циклогексаноне. Зависимость. от концентрации циклогексанона при различных температурах. [37] |
В таком комплексе под влиянием водородных связей облегчается разрыв связи О-О в гидроперекиси, приводящий к образованию свободных радикалов. [38]
В таком комплексе под влиянием водородных связей облегчается разрыв связи О-О в гидроперекиси, приводящий к образованию двух свободных радикалов. При этом молекула кислоты регенерируется. [39]
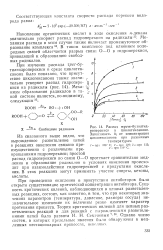 |
Распад mpem - бутилгид-роперекисн в циклогексаноне. Зависимость k, от концентрации циклогексанона при различных температурах. [40] |
В таком комплексе под влиянием водородных связей облегчается разрыв связи О-О в гидроперекиси, приводящий к образованию свободных радикалов. [41]
Необходимо рассмотреть вопрос о влиянии водородной связи на ХС и КССВ, поскольку этим в значительной степени определяется характеристичность параметров ЯМР. [42]
Для подтверждения наших предположений относительно влияния водородных связей в замещенных фенола на процесс поликонденсации с формальдегидом были проведены исследования реакции поликонденсации орто - и парапитрофеполов, о которых нет данных в литературе. Общепринятым является мнение, что ортонитрофенол не образует смолы поликонденсацией с формальдегидом. Действительно, все паши попытки получить смолу на основе ортонитрофенола не увенчались успехом. Исследование проводилось в присутствии кислых и щелочных катализаторов при 80 - 120 в течение 48 - 60 часов. Только в результате поликонденсации ортонитрофенола г формальдегидом, проводимой в течение 6 часов при 80 - 90 в присутствии аммиака, взятого в эквимолекулярном количестве по отношению к нитрофенолу, образовалась смола, нерастворимая в воде и кислотах и легко растворимая в разбавленных щелочах. Возможно, что аммиак своим присутствием экранирует нитрогруппу и нарушает ее влияние на гидроксильную группу фенола. Паранитрофенол образует с формальдегидом в присутствии как щелочей, так и кислот, взятых в реакцию в количестве 1 5 - 2 % от веса нитрофенола, водостойкие и кислотостойкие смолы. Наряду с этим известно, что ортохлорфеполы и ортоалкилфенолы, не имеющие внутримолекулярных водородных связей, реагируя с формальдегидом, образуют смолы новолачного типа. [43]
Наиболее подходящим примером, иллюстрирующим влияние водородных связей между молекулами реагента и растворителя на скорость реакции, является изученное Хартом и сотрудниками [51] ингибирование эфирами алкилирования фенолов. [44]
Частота этой полосы заметно подверждена влиянию водородной связи, вследствие чего возможны значительные смещения при переходе от твердого состояния к раствору. Это же относится ( и даже в большей степени) к другим характеристическим полосам амидов; поэтому при работе с амидами и другими подобными веществами особое внимание должно быть обращено на агрегатное состояние, в котором исследуется вещество. Кроме полосы поглощения карбонильной группы, первичные и вторичные амиды имеют характеристические полосы, обусловленные колебаниями NH. Эти полосы в совокупности с первой полосой обычно вполне характеризуют амидную группировку. У первичных амидов имеются две формы деформационных колебаний NH, соответствующие антисимметричным и симметричным колебаниям водородных атомов, в то время как у вторичных амидов обычно имеется только одиночная полоса, положение которой зависит от того, существует ли данное соединение в цис - или транс-форме. Образование водородной связи опять-таки приводит к значительным смещениям частот в спектре вещества в твердом состоянии, а для концентрированных растворов часто можно наблюдать полосы колебаний одновременно как свободных, так и связанных групп NH. Положение полос, относящихся к колебаниям связанных групп NH, меняется также в зависимости от природы образующихся водородных связей; имеются, например, различия между частотами колебаний связанных групп NH вторичных амидов в цис - и транс-формах. В спектрах многих вторичных амидов вторая полоса поглощения NH находится при меньших частотах, а у более сложных веществ, таких, как полипептиды и белки, в этой области имеется несколько полос поглощения. Например, дике-топиперазин в твердом состоянии имеет пять полос, причем все они, по-видимому, связаны с валентными колебаниями NH. Интерпретация этих сложных полос рассматривается в разделе, посвященном полипептидам и белкам. Следует, однако, заметить, что имеются отчетливые различия в поведении ОН-и NH-групп при изменении состояния вещества. [45]
Страницы: 1 2 3 4