Влияние - электростатическая сила
Cтраница 2
Рэлей впервые заметил, что дробление струи водяного фонтана уменьшается под влиянием электростатических сил. Он, однако, не исследовал достаточно детально этого явления и не предложил удовлетворительной теории для его объяснения. [16]
Продукты гидролиза и гидратации, первоначально возникшие в коллоидной форме, под влиянием молекулярных, сорб-ционных и электростатических сил уплотняются, коагулируют. [17]
Известно, что в водных растворах сильные электролиты полностью диссоциируют, но под влиянием электростатических сил притяжения и отталкивания происходит интенсивное влияние противоположно заряженных ионов. [18]
Слой диэлектрического материала, нанесенный - на поверхность частиц, способствует агломерации частиц под влиянием электростатических сил, что в свою очередь приводит к изменению структуры кипящего слоя и к уменьшению коэффициента теплоотдачи. Численные значения коэффициента теплоотдачи в результате расчета по опытным данным оказались з пределах: для песка - от 318 до 515 Ккал / м2час С и для катализатора - от 244 до 420 ккал / м2час С. [19]
Наряду с этими универсальными силамл притяжения возможен также яш-дущиоллый эффект, возникающий в результате деформации молекул иод влиянием электростатических сил соседних молекул. [20]
Величина коэффициента активности зависит от валентности ионов и от так называемой ионной силы раствора, которая характеризует степень влияния электростатических сил между ионами и в свою очередь зависит от общего количества находящихся в растворе ионов и их валентности. [21]
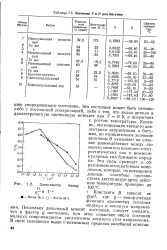 |
Значения А и В для битумов. [22] |
Конечно, эта концепция твердого диэлектрика неприменима к битумам, но отрицательное значение величины В указывает на сильное взаимодействие между его молекулами под влиянием электростатических сил и межмолекулярных сил ближнего порядка. Эти силы приводят к образованию ассоциативных комплексов, которые, по имеющимся данным, способны противостоять диссоциирукщему действию температуры примерно до 100 С. [23]
Притяжение двух диполь-ных молекул, обязанное так называемому ориентационному эффекту, пропорционально ji4, где ji - дипольный момент. Следовательно, влияние электростатических сил быстро возрастает с увеличением диполь-ного момента. [24]
Это показывает, что влияние электростатических сил играет важную роль в явлении высаливания. Значение величин ионных радиусов неясно, и сделанное на основании теории предположение о последовательности величин солевого эффекта для разных солей не совпадает с наблюдаемыми результатами. Эти расхождения могут быть частично устранены, если ограничить исследования разбавленными растворами как солей, так и нейтральных молекул. [25]
Эти электростатические силы оказывают значительное влияние на конформацию макроионов в растворе и на химическое соединение макроионов с другими ионами, в том числе на их кислотные и основные свойства. Отсюда вытекает необходимость довольно подробно рассмотреть влияние электростатических сил. [26]
В центральной части капилляра, вне пределов двойного электрического слоя, числа переноса будут такие же, как и в сво -, бодном растворе без мембраны, так как подвижности и концентрации ионов ра-створа, наполняющего капилляр в центральной части и в свободном растворе, одинаковы. В цилиндрической оболочке, входящей в двойной слой, вследствие влияния электростатических сил поверхности, подвижности и концентрации находящихся там ионов будут отличаться от свободного раствора и поэтому числа переноса в этом слое будут иные, чем в свободном растворе. [27]
Различное значение величин Т и Г0, несмотря на предполагаемую полную диссоциацию электролита, объясняется данной теорией тем, что, хотя молекулы и диссоциированы полностью на ионы, последние, однака, не являются вполне кинетически свободными. Они не дают ожидаемого осмотического действия, так как под влиянием электростатических сил между заряженными ионами, или так называемых ин-терионных сил, они мешают друг другу, взаимно связывая свободу действий. [28]
 |
Длины связей н величины dr - р - перекрывания в ионах ХО. [29] |
Однако, возможно, этого недостаточно, так как в SF3N [ где S-N - связь должна быть ближе к тройной, нежели к двойной связи ( см. стр. Связь часто оказывает влияние на конфигурацию молекулы, хотя в некоторых случаях нельзя не учитывать влияния электростатических сил. Хорошо известный пример плоской 513М - группировки в ( SiH3) 3N подробно рассмотрен на стр. Валентный угол у атома кислорода в разных ХОХ-мостиковых системах также указывает на изменяющуюся степень я-связи X-О. Так, если величина этого угла относительно мала ( - 120е), только одна пара электронов атома кислорода ориентирована так, что образуется я-связь с d - орбиталями атомов X, в то время как в предельном случае ( угол ХОХ 180) возможно образование двух я-связей. [30]
Страницы: 1 2 3 4