Влияние - электростатическая сила
Cтраница 3
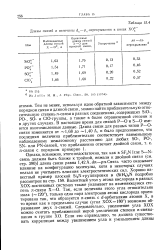 |
Длины связей и величины dr - р - перекрывапия в ионах ХО. [31] |
Однако, возможно, этого недостаточно, так как в SF3N [ где S-N - связь должна быть ближе к тройной, нежели к двойной связи ( см. стр. Связь часто оказывает влияние на конфигурацию молекулы, хотя в некоторых случаях нельзя не учитывать влияния электростатических сил. Хорошо известный пример плоской SigN-группировки в ( SiH3) 3N подробно рассмотрен на стр. Валентный угол у атома кислорода в разных ХОХ-мостиковых системах также указывает на изменяющуюся степень л-связи X-О. Так, если величина этого угла относительно мала ( - 120), только одна пара электронов атома кислорода ориентирована так, что образуется я-связь с d - орбиталями атомов X, в то время как в предельном случае ( угол ХОХ180) возможно образование двух л-связей. [32]
По представлениям В. Н. Неберы [17], знак и величина заряда, а не химическая природа иона, имеют решающее значение для адсорбции. Если коллоидные частицы и молекулы флокулянта имеют противоположный по знаку заряд, то полимер под влиянием электростатических сил адсорбируется на поверхности частиц, вытесняя оттуда находящиеся в адсорбционном слое ионы простых электролитов. Это вытеснение происходит благодаря большему электрическому заряду полимера по сравнению с зарядом простых ионов. [33]
Как уже указывалось, концентрацию С вычисляют для сильных электролитов, исходя из допущения полной диссоциации их в растворе. Что же касается коэффициента активности, то согласно современной теории сильных электролитов он представляет собой меру влияния электростатических сил притяжения и отталкивания, действующих между ионами, на способность иона к химическим действиям. Если fa 1, это значит, что ион стеснен в своих движениях межионными силами. [34]
Как уже указывалось, концентрацию С вычисляют для сильных электролитов, исходя из допущения почти полной диссоциации их в растворе. Что же касается коэффициента активности, то, согласно современной теории сильных электролитов, он представляет собой меру влияния электростатических сил притяжения и отталкивания, действующих между ионами, на способность иона к химическим действиям. Если / а1, это значит, что и он стеснен в своих движениях междуионными силами. Это значит, что ион действует соответственно своей концентрации в растворе. Точно так же можно не считаться с междуионными силами и в случае не слишком концентрированных растворов слабых электролитов, у которых только ничтожная часть всех молекул диссоциирована на ионы. [35]
Как уже указывалось, концентрацию С вычисляют для сильных электролитов, исходя из допущения почти полной диссоциации их в растворе. Что же касается коэффициента активности, то, согласно современной теории сильных электролитов, он представляет собой меру влияния электростатических сил притяжения и отталкивания, действующих между ионами, на способность иона к химическим действиям. Если / а1, это значит, что ион стеснен в своих движениях междуионными силами. Это значит, что ион действует соответственно своей концентрации в растворе. Точно так же можно не считаться с междуионными силами и в случае не слишком концентрированных растворов слабых электролитов, у которых только ничтожная часть всех молекул диссоциирована на ионы. [36]
Как уже указывалось, концентрацию С вычисляют для сильных электролитов, исходя из допущения почти полной диссоциации их в растворе. Что же касается коэффициента активности, то, согласно современной теории сильных электролитов, он представляет собой меру влияния электростатических сил притяжения и отталкивания, действующих между ионами, на способность иона к химическим дйствиям. Если / а1, это значит, что ион стеснен в своих движениях междуионными силами. Это значит, что ион действует соответственно своей концентрации в растворе. Точно так же можно не считаться с междуионными силами и в случае не слишком концентрированных растворов слабых электролитов, у которых только ничтожная часть всех молекул диссоциирована на ионы. [37]
Ионы Na и К гочти не адсорбируются, поскольку КНП для них очень велика ( частицы заряжены отрицательно), адсорбция под действием электростатических сил не происходит. Почти такая же картина наблюдается и для ионов Li, Са241, Ва2, однако при одинаковых значениях рН величина адсорбции двухзарядных ионов несколько больше, что связано с влиянием электростатических сил. Адсорбция ионов Cu2, Ni2, Со2 начинается в области левее КНП ( заряд частиц положителен), и обусловлена она действием не только электростатических, но и химических сил. Адсорбция ионов Си2 и Ni начинается с рН 0 5, когда электростатическое отталкивание и химическое адсорбционное взаимодействие уравновешиваются. Определяя по уравнению (4.28) величину ф, мы получим ф, равный - 80 мВ, или - 7 95 кДж / моль. Для ионов Си присутствие в системе 0 1 MNaCl оказывает заметное влияние на процесс хемосорбции. Чтобы электронейтральность раствора сохранялась, в процессе адсорбции ионы водорода не должны переходить в раствор. Однако эксперименты показывают, что в ходе адсорбции рН раствора уменьшается. Поскольку одновременная адсорбция катиона и аниона в данном случае невозможна, то ионный обмен должен сопровождаться переходом Н в раствор. [38]
Получения фосфорной кислоты, в реакционной суспензии кристаллизуется сульфат кальция в виде двухводной, полуводной или безводной соли. На зернах апатита может появляться сульфатная корка вследствие прилипания к ним значительно меньших по размеру ( Ю-15 мкм) шламовых кристаллов полугидрата сульфата кальция CaSO4 - 0 5H2O или ангидрита CaSO4 под влиянием молекулярных и электростатических сил притяжения. Кристаллы крупнее 30 - 40 мкм, близкие по размерам к зернам апатита, почти не прилипают к их поверхности и не образуют шламового покрова. [39]
Co ( NH3) 5NO2 ] SO4 константа ассоциации, вычисленная путем измерения проводимости, значительно выше, чем наблюдаемая в растворах 2: 2-электролитов, содержащих малые ионы. Так как ассоциация под влиянием чисто электростатических сил должна уменьшаться при увеличении размеров ионов, предположили, что дисперсионные силы, действующие между катионом и анионом, в сильной мере определяют ассоциацию IB растворах, содержащих комплексные ионы, поскольку дисперсионные силы в первом приближении не зависят от заряда. [40]
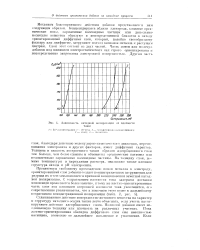 |
Зависимость катодной поляризации от плотности тока. [41] |
Механизм благоприятного действия добавок представляется нам следующим образом. Слой этот со стоит из двух частой. Часть ионов или молекул добавки под влиянием электростатических сил строго ориентирована и непосредственно закреплена электродной поверхностью. [42]
В псевдоожиженном слое, несмотря на тенденцию к сохранению среднего расстояния между частицами, всегда возможно возникновение отдельных областей повышенной порозности. Это может явиться следствием беспорядочной начальной укладки частиц или влияния электростатических сил и сил трения при псевдоожижении. Области повышенной порозности непрерывно возникают над газораспределительной решеткой также по той причине, что твердая фаза периодически перекрывает сечение для прохода газа. Возникающие при этом колебания газовых струй из отдельных отверстий не совпадают по фазе, поэтому общая пульсация газового потока выражена гораздо слабее. [43]
Эти модели, очевидно, не вполне соответствуют реальной картине, создающейся в такой сложной ситуации. Тем не менее эти пути логически непротиворечивы и позволяют оценить влияние электростатических сил на константы диссоциации ряда ионизирующихся групп, не образующих водородных связей. Приближенность вычислений не позволяет сделать однозначный вывод о том, что образование водородной связи в рассмотренных случаях несущественно, однако становится очевидной необходимость ряда независимых доказательств при установлении наличия водородной связи в этих соединениях. [44]
Если полярную молекулу ( диполь) поместить в электрическое поле, то она ориентируется таким образом, чтобы ее положительный полюс был направлен к внешнему отрицательному полюсу ( фиг. При этом, если полярная молекула имеет шаро-образую форму и расстояния полюсов от центра шара одинаковы, то произойдет поворот молекулы вокруг ее оси, как это показано на фиг. Если же полярная молекула не имеет формы шара, то вся молекула, под влиянием электростатических сил, воздействующих на оба ее полюса, переместится и примет ту ориентацию, которая показана на фиг. Время, необходимое для осуществления подобного перемещения, можно определить, изменяя частоту внешнего переменного электрического поля. [45]
Страницы: 1 2 3 4