Влияние - диффузионный фактор
Cтраница 2
 |
Прибор для определения скорости реакции восстановления окислов металлов. [16] |
Скорость восстановления контакта необходимо изучать при заданном температурном режиме, исключив влияние диффузионных факторов на истинную скорость кристаллохимического превращения окисла в металл. [17]
Сложность изучения кинетики химической стадии экстракции заключается в том, что для исключения влияния диффузионных факторов на общую скорость процесса необходимо применять интенсивное перемешивание, а в связи с этим возникает задача обеспечения минимального времени контакта двух быстро перемешивающихся фаз. Эти трудности были преодолены при Проведении опытов по описанной ниже методике. [18]
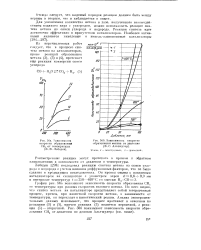 |
Зависимость скорости. [19] |
Лебедев [298] исследовал реакцию синтеза метана из окиси углерода и водорода с учетом влияния диффузионных факторов, что не было сделано в предыдущих исследованиях. [20]
При определении Ki, а из VR, i хроматографический опыт стараются проводить так, чтобы влияние кинетических и диффузионных факторов на хроматограмму было бы как можно меньше. Иными словами, в этом опыте стремятся приблизиться к предельному случаю идеальной хроматографии. С этой целью, во-первых, стараются сократить пути внутренней диффузии при-использовании непористых или макропористых адсорбентов с возможно более однородной поверхностью, близкими и небольшими ( однако не вызывающими чрезмерного повышения давления у входа в колонну) размерами зерен правильной формы и равномерной их упаковкой. [21]
Переходными диффузионными областями в кинетике гетерогенных каталитических реакций обычно называют режимы их протекания, в границах которых влияние диффузионных факторов становится достаточно заметным и искажающим основные закономерности, но не превалирующим. [22]
Козлов проследил изменение энергии активации на всем протяжении процесса, однако выбранная им методика исследования не позволяла исключать влияние диффузионных факторов на скорость реакции. Окись металла и углерод загружались толстым слоем в кварцевую чашечку, и продукты реакции должны были диффундировать к внешней поверхности слоя. Поэтому его выводы нельзя считать полностью достоверными, особенно там, где указывается, что даже в начальной стадии при малых степенях восстановления МпСЬ и Мг Оз скорость процесса описывается параболическим уравнением. [23]
Концентрация бензола все время постоянна и высока, так как выделение тиофена производится из среды бензола и поэтому влияние диффузионных факторов на сульфирование бензола будет меньше, чем на сульфирование тиофена. [24]
Результаты работ Чуфарова с сотрудниками по определению пористости окислов железа в процессе восстановления [11, 12] также позволяют судить о влиянии диффузионных факторов на скорость процесса. Было установлено, что пористость окислов железа, а следовательно, и скорость их восстановления значительно уменьшаются при высоких температурах. [25]
Как уже отмечалось, каждый из перечисленных признаков сам по себе не всегда может быть достаточным основанием для однозначного суждения о влиянии диффузионных факторов. Так, даже влияние изменений размеров гранул катализатора на скорость реакции может быть вызвано разной степенью их восстановления. Наличие изломов Аррени-усовских прямых может быть следствием изменения механизма реакции в кинетической области, а не влияния диффузии. Поэтому суждение о влиянии диффузионных факторов будет более надежным, если оно сделано на основании совокупности разных данных. [26]
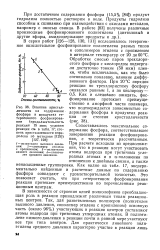 |
Влияние кристалличности на содержание фосфора в продуктах гетерогенного фосфонирова-ния ( продолжительность реакции 15 мин. условия реакции в 17. степень кристалличности определена по методике. [27] |
Обработке смесью паров треххлори-стого фосфора с кислородом подвергали достаточно тонкие ( 50 мкм) пленки, чтобы исключалось, как это было специально показано, влияние диффузионного фактора. [28]
По данным Г. М. Панченкова и Н. В. Голованова [44], реакция окисления коиса на катализаторах с содержанием более 4 % переходит во внутридиффузионную область при температуре 520 - 530 С. Влияние диффузионных факторов на скорость регенерации слабо закоксованных катализаторов ( менее 1 63 % кокса) не было замечено при температурах вело до 600 ( С. [29]
Свободные радикалы, получаемые при распаде слабых звеньев надмолекулярных структур, обладающие еще большей степенью делокализации неспаренного электрона и диффузионными затруднениями к перемещению, могут иметь еще меньшую активность, чем аллильный радикал. Влияние диффузионных факторов на активность малоактивного радикала впервые было показано Шмидтом [77], применившим для стабилизации радикалов стеклообразную массу. [30]
Страницы: 1 2 3 4