Влияние - электролит
Cтраница 1
Влияние электролитов и карбоксиметилцеллюлозы на прочность структуры в системах глина - жидкость. [1]
Влияние электролитов на адсорбцию радиоактивных изотопов зависит не только от природы электролита, но и от состояния радиоактивного изотопа в растворе. [2]
Влияние электролитов на скорость седиментации грубых суспензий аналогично влиянию их на скорость коагуляции коллоидных растворов. [3]
Влияние электролитов на адсорбцию радиоактивных изотопов зависит не только от природы электролита, но и от состояния радиоактивного изотопа в растворе. [4]
Влияние электролитов на набухание полимеров рассмотрено ниже в разд. [5]
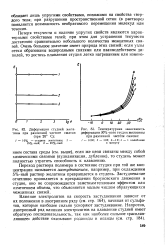 |
Деформация студней желатины при различной частоте сжатия.| Температурная зависимость. [6] |
Влияние электролитов на скорость застудневания зависит от их положения в лиотропном ряду ( см. стр. Напротив, лиотропный ряд влияния электролитов на плавление студней имеет обратную последовательность, так как наиболее сильное расплавляющее действие оказывают роданиды и иодиды ( см. стр. [7]
Влияние электролитов на ККМ в растворах неионогенных ПАВ обусловлено эффектом высаливания, так как между влиянием ионов на ККМ неионогенных ПАВ и их положением в лиотропном ряду существует четкий параллелизм. [8]
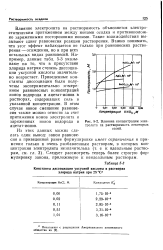 |
Влияние концентрации электролита на растворимость некоторых солей. [9] |
Влияние электролита на растворимость объясняется электростатическим притяжением между ионами осадка и противоположно заряженными посторонними ионами. Такие взаимодействия вызывают сдвиг равновесия реакции растворения. Важно понимать, что этот эффект наблюдается не только при равновесиях растворения - осаждения, но и при всех остальных видах равновесий. Например, данные табл. 5 - 3 указывают на то, что в присутствии хлорида натрия степень диссоциации уксусной кислоты значительно возрастает. Приведенные константы диссоциации были получены экспериментально измерением равновесных концентраций ионов водорода и ацетат-ионов в растворах, содержащих соль в указанной концентрации. [10]
 |
Схематический ход кривой 0 этим минимальна и степень. [11] |
Влияние электролитов ( точнее-нейтральных солей) также хорошо изучено для белков и целлюлозы. Влияние это своеобразно прежде всего тем, что принадлежит главным образом анионам и лишь в незначительной мере катионам. Своеобразно и то, что одни анионы усиливают набухание, тогда как другие ослабляют его, причем усиливающее или ослабляющее действие для различных анионов различно. [12]
Влияние электролитов, не содержащих общего кона с осадком, на растворимость осадка особенно заметно, когда в состав осадка входят многозарядные ионы, так как коэффициент активности многозарядных ионов более резко уменьшается при увеличении ионной силы раствора. [13]
Влияние электролитов, не содержащих общего иона с осадком, на растворимость осадка особенно заметно, если в состав осадка входят многозарядные ионы, так как коэффициент активности многозарядных ионов более резко уменьшается при увеличении ионной силы раствора. [14]
Влияние электролита на структуру раствора не ограничивается сольватацией ионов. Оно также может играть роль в изменении структуры самого растворителя. Таким образом, в величинах химического сдвига в спектрах ЯМР проявляются оба этих эффекта. Химический сдвиг воды в этой системе дает относительно небольшую информацию об отдельном сольватацион-ном эффекте, поскольку добавление ацетонитрила разрушает Н - свя-занную структуру воды, а это приводит к сдвигу в спектре ЯМР в противоположном направлении, чем при координации молекул воды ионами серебра. Более существенная информация о составе сольвата извлекается из химического сдвига ацетонитрила. В соответствии с результатами потенциометрического титрования она показывает, что молекулы ацетонитрила координируются в первой координационной сфере иона серебра. [15]
Страницы: 1 2 3 4