Влияние - электролит
Cтраница 2
Влияние электролитов также хорошо изучено для белков и целлюлозы. На процесс набухания оказывают влияние, главным образом, анионы, причем влияние последних своеобразно. Одни из них усиливают набухание, другие ослабляют. [16]
Влияние электролитов на термодинамический и электрокинетический потенциалы. Термодинамический потенциал, как мы знаем, определяется разностью потенциалов, создаваемых поверхностно ядерными ионами, с одной стороны, и суммарным зарядом всех противоионов - с другой. В нашем примере ( золь As2S3) это будет разность потенциалов между зарядами nHS - п и пН - - / г, При изменении концентрации электролита в жидкой фазе величина п почти не изменяется. Именно поэтому прибавление к золю электролитов почти не влияет на величину термодинамического потенциала. [17]
 |
Знак заряда мицеллярного остова в гидрозолях различных веществ. [18] |
Влияние электролитов на термодинамический и электрокинетический потенциалы. Термодинамический скачок потенциала, как мы знаем, определяется разностью потенциалов, создаваемых поверхностно ядерными ионами, с одной стороны, и суммарным зарядом всех противоионов - с другой. При изменении концентрации электролита в жидкой фазе величина п почти не изменяется. Именно поэтому прибавление к золю электролитов почти не влияет на величину термодинамического потенциала. [19]
Влияние электролитов на ККМ, Наличие солей в растворе понижает критическую концентрацию мицеллообразования, степень понижения в каждом случае зависит, главным образом, от концентрации прибавленного электролита и заряда его иона, противоположного по знаку заряду мицеллы. [20]
Влияние электролитов на солюбилизацию полярных органических веществ неоднозначно, однако в большинстве случаев электролиты понижают их растворимость, в отличие от углеводородов. Это объясняется различиями в способах включения полярных и неполярных молекул в мицеллы. Понижение степени дисперсности мицеллярного раствора под влиянием электролитов уменьшает суммарную площадь поверхностного слоя мицелл, в котором происходит локализация полярных молекул, что влечет за собой уменьшение солюбилизирующей способности по отношению к олеофиль-ным веществам полярного характера. [21]
Влияние электролитов на скорость седиментации грубых суспензий аналогично влиянию их на скорость коагуляции коллоидных растворов. [22]
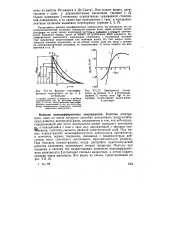 |
Влияние неиндиффе - [ IMAGE ], 17. Зависимость потен-рентного электролита на q0 - и. - циала ф0 ( кривая / и - потенциала потенциалы. ( кривая 2 частиц золя Agl от ло. [23] |
Влияние электролита, один из ионов которого способен достраивать кридталличе-скую решетку дисперсной фазы, заключается в том, что потенциал-определяющий ион этого электролита может повышать потенциал гсо, а находящийся с ним в паре ион, одноименный с зарядом про-т ЙЪоиона, способен сжимать двойной электрический слой. При малых концентрациях неиндифферентного электролита проявляется, в основном, первая тенденция, связанная с поверхностным действием иона, способного достраивать кристаллическую решетку. При больших концентрациях, когда достройка кристаллической решетки завершена, превалирует вторая тенденция. [24]
Влияние электролитов на набухание полимеров рассмотрено ниже в разд. [25]
Влияние электролитов на процесс гидратообразования объясняется как высаливание. Высаливающее влияние отдельных ионов растет с их зарядом и зависит от радиуса иона. [26]
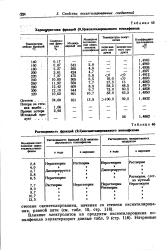 |
Растворимость фракций ( 9 5 оксимепимроваиного нонилфенола. [27] |
Влияние электролитов на продукты оксиэтилирования нонилфенола характеризуют данные табл. 9 ( стр. [28]
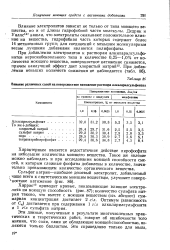 |
Влияние различных солей на поверхностное натяжение раствора алкиларилсульфоната. [29] |
Влияние электролитов зависит не только от типа моющего вещества, но и от длины гидрофобной части молекулы. Дедрик и Уилле1 7 нашли, что электролиты оказывают положительное влияние на вещества, гидрофобная часть которых содержит более 14 метиленовых групп; для соединений с меньшим молекулярным весом лучшими добавками являются полифосфаты. [30]
Страницы: 1 2 3 4