Влияние - посторонний электролит
Cтраница 1
Влияние посторонних электролитов на застудневание весьма сложно. По своему влиянию анионы можно расположить в аналогичный ряду высаливания - ряд застудневания. [1]
Влияние посторонних электролитов на застудневание весьма сложно. По своему влиянию анионы можно расположить в аналогичный ряду высаливания-ряд застудневания. [2]
Влияние посторонних электролитов на застудневание весьма сложно, особенно если электролит вступает с коллоидными частицами в химическое взаимодействие. [3]
 |
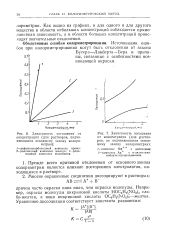
Влияние концентрации. [4] |
Под влиянием посторонних электролитов происходит деформация молекул или заряженных частиц поглощающего вещества, что приводит к изменению спектра поглощения этого вещества. [5]
Другая сторона влияния постороннего электролита состоит в уменьшении диэлектрической проницаемости водной фазы, что приводит к изменению константы диссоциации реагента и константы устойчивости комплекса. Изменяются и константы распределения, которые зависят от ионной силы раствора. Суммарный результат действия солей предсказать довольно трудно. Физическая химия накопила значительный материал о коэффициентах активности неэлектролитов в растворах электролитов [52, 53], но эти данные учитывают не все стороны процессов, протекающих при экстракции внутрикомплекеных соединений. [6]
Прежде всего сказывается влияние посторонних электролитов в растворе, которые вызывают деформацию электронных оболочек образующегося окрашенного соединения, в результате чего меняется его светопоглощаемость. Поэтому наиболее точные результаты анализа получаются в том случае, когда посторонние ионы или удаляют, или делают приблизительно одинаковыми концентрации их в исследуемом и стандартном ( образцовом) растворах. [7]
Нужно различать два случая влияния постороннего электролита на растворимость малорастворимой соли. В первом случае растворимый электролит не имеет одноименных иолов с малорастворимым электролитом и влияет на его средний коэффициент активности. [8]
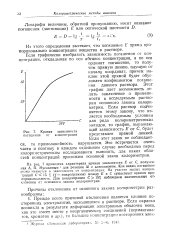 |
Кривая зависимости погашения от концентрации. [9] |
Прежде всего причиной отклонения является влияние посторонних электролитов, находящихся в растворе. [10]
Естественно, установление основных закономерностей влияния посторонних электролитов на растворимость насыщающих раствор солей, в условиях постоянства коэффициента активности, не умаляет значения этой величины, так как во всех наших уравнениях ( 7, 11, 14) фигурирует концентрация соли в молярных долях, а она коррелируется коэффициентом активности. [11]
Рассмотрим несколько примеров вычислений, которыми характеризуется влияние посторонних электролитов на растворимость осадков. [12]
В данной работе представлены теоретические выводы закономерностей влияния посторонних электролитов на растворимость солей, которые, как это ни парадоксально, установлены именно в условиях постоянства коэффициентов активности. [13]
В реакциях, протекающих с участием слабых электролитов, влияние посторонних электролитов может проявляться в форме так называемого вторичного солевого эффекта. Так, например, реакция инверсии сахара катализируется ионами водорода. [14]
Страницы: 1 2 3