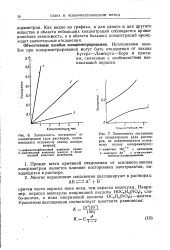
Влияние - посторонний электролит
Cтраница 2
Прежде всего причиной отклонения от основного закона колориметрии является влияние посторонних электролитов, находящихся в растворе. [16]
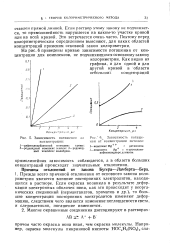 |
Зависимость погашения от концентрации.| Зависимость погашения от концентрации металла. [17] |
Прежде всего причиной отклонения от основного закона колориметрии является влияние посторонних электролитов, находящихся в растворе. Если окраска возникла в результате деформации электронных оболочек иона, как это происходит у неорганических соединений ( перманганатов, хроматов и др.), то большие концентрации посторонних электролитов изменяют деформацию, следствием чего является изменение поглощаемости света, и следовательно, погашение изменяется. [18]
Прежде всего причиной отклонения от основного закона колориметрии является влияние посторонних электролитов, находящихся в растворе. [20]
В реакциях, протекающих с участием слабых электролитов, влияние посторонних электролитов может проявляться в форме так называемого вторичного солевого эффекта. Так, например, реакция инверсии сахара катализируется ионами водорода. [21]
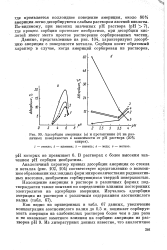 |
Адсорбция америция ( а и протактиния ( б на различных поверхностях в зависимости от рН раствора ( 20 %. [22] |
Нахождение америция в растворе в различных формах подтверждается также опытами по определению влияния посторонних электролитов на адсорбцию америция. [23]
 |
Результаты измерения коэффициентов активности солей ( f. [24] |
Применимость закона ионной силы к разбавленным растворам сильных электролитов объясняет опытные данные по влиянию посторонних электролитов на растворимость малорастворимых солей. [25]
Рассмотрение характера изменения растворимости насыщающих растворы солей, при условиях постоянства рационального коэффициента активности и молярной доли, приводит к установлению всех закономерностей влияния посторонних электролитов на растворимость насыщающих растворы солей, которые были открыты в результате многолетних экспериментальных исследовании большого числа ученых. [26]
По заданию преподавателя работа может быть видоизменена, например: 1) определить числа переноса в зависимости от концентрации электролита; 2) исследовать влияние посторонних электролитов на числа переноса; 3) определить числа переноса в комплексных растворах. [27]
Из числа внешних факторов, влияющих на формирование осадка отдельных катионов, учитывались следующие: 1) изменение температуры, 2) величина физической сорбции ионов бумагой, 3) влияние посторонних электролитов, 4) взаимодействие определяемого иона с растворителем, 5) взаимодействие данного осадка с другим осадком, 6) изменение рН среды. [28]
 |
Водородный электрод с подвижной водородной атмосферой.| Водородный электрод с неподвижной водородной атмосферой. [29] |
В щ лочных растворах происходит разложение вследствие окисления и поэтому падение потенциала. В растворах с концентрацией электролита выше нормальной хингидронный электрод дает неверные показания на несколько милливольт, так как влияние посторонних электролитов на растворимость компонентов хинон-гидрохинон - различно. [30]
Страницы: 1 2 3