Влияние - посторонний электролит
Cтраница 3
Молярная доля соли или иона и многокомпонентной системе может оставаться постоянной при заметных изменениях состава раствора. На чтом основании рассмотрен характер изменения растворимости солей в условиях постоянства рационального коэффициента активности ( i), молярной доли ( N) и установлены закономерности влияния посторонних электролитов на растворимость насыщающих растворы солей - Выведенные уравнения и па основании их установленные закономерности теоретически обосновывают все эмпирические закономерности, которые были открыты в результате многолетних экспериментальных исследований большого числа ученых и конне прошлого и и начале настоящего столетия. [31]
Ясно, что в свою очередь ионы серебра и хлорид-ионы также испытывают взаимное притяжение. Эти ионные - атмосферы частично нейтрализуют заряд иона серебра и хлорид-иона и таким образом уменьшают их взаимное притяжение. Если сила притяжения между Ag и С1 - в азотной кислоте меньше, чем в чистой воде, то растворимость хлорида серебра в азотной кислоте должна быть больше. Это заключение является правильным; такая простая картина помогает предсказать влияние посторонних электролитов на химическое равновесие. [32]
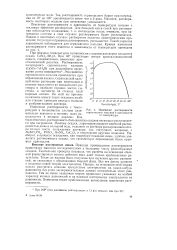 |
Изменение растворимости. [33] |
Такие же выводы были получены при изучении других равновесий, не связанных с образованием твердой фазы. Правда, на основании этой теории нельзя рассчитать влияние присутствия электролитов на какое-нибудь равновесие без ряда экспериментальных данных относительно этого равновесия. Тем не менее названная теория правильно указывает на особый характер ионных равновесий и на влияние посторонних электролитов на равновесие. Возможны также приближенные вычисления изменения растворимости. [34]
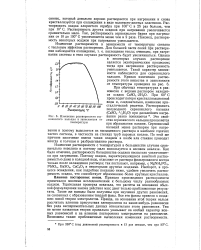 |
Изменение растворимости сернокислого кальция в зависимости от температуры. [35] |
Изменение растворимости с температурой в большинстве случаев сравнительно невелико и поэтому мало используется в весовом анализе. Как было отмечено, растворимость большинства осадков несколько увеличивается при нагревании. Поэтому осадки, характеризующиеся заметной растворимостью даже в холодной воде, отделяют от раствора фильтрованием всегда только после охлаждения раствора; так поступают, например, с MgNH4PO4, PbSO4, BaSO4, CaC2O4 и некоторыми другими осадками. Наоборот, в процессе осаждения, как подробнее показано ниже, удобнее увеличить растворимость осадка, что способствует образованию более крупных кристаллов. Такие же выводы были получены при изучении других равновесий, не связанных с образованием твердой фазы. Правда, на основании этой теории нельзя рассчитать влияние присутствия электролитов на какое-нибудь равновесие ез ряда экспериментальных данных относительно этого равновесия. Тем не менее названная теория правильно указывает на особый характер ионных равновесий и на влияние посторонних электролитов на равновесие. Возможны также приближенные вычисления изменения растворимости. [36]
Страницы: 1 2 3