Влияние - карбонильная группа
Cтраница 3
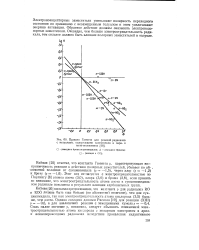 |
Правило Гаммета для реакций радикалов. [31] |
Этот ход согласуется с электроогрицательностью по Паулингу [8] атомов азота ( 3 0), хлора ( 3 0) и брома ( 2 8), если принять во внимание, что электроотрицателыюсть атома азота в сукцинимидиль-ном радикале повышена в результате влияния карбонильных групп. [32]
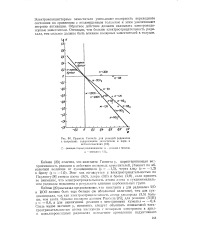 |
Правило Гаммста для реакций радикалов с толуолами, содержащими заместители в пара - и. [33] |
Этот ход согласуется с электроотрицательностью по Паулингу [8] атомов азота ( 3 0), хлора ( 3 0) и брома ( 2 8), если принять во внимание, что электроотрицательность атома азота в сукцинимидиль-ном радикале повышена в результате влияния карбонильных групп. [34]
В то же время различия в электроотрицательностях атомов С, N и О и в поляризуемости связей С О, N - О и C N, а также то, что в полициклических хинонах атом углерода группы СО входит непосредственно в циклическую сопряженную систему, тогда как атомы азота групп NO2 и NO лишь подключены к такой системе, а сами в нее не входят, обусловливают различия во влиянии карбонильной группы и ее гетероаналогов на распределение я-электронной плотности в молекулах. [35]
Метод, как видно, весьма близок только что описанному. Влияние карбонильной группы обусловливает реакционноспособность определенного места ядра. [36]
Соединения с активной карбонильной группой мешают определению воды, образуя при взаимодействии с метанолом ацетали и кетали. Влияния карбонильной группы можно избежать, добавляя цианистый водород, который образует циангидрины, не мешающие определению. Из других веществ, оказывающих мешающее действие, можно назвать меркаптаны и некоторые амины, реагирующие с иодом, а также различные окислители, такие как пероксид-ные кислоты, диацилпероксиды и хиноны, реагирующие с иодидом с образованием свободного иода. [37]
Метод, как видно, весьма близок только что описанному. Влияние карбонильной группы обусловливает реакционноспособность определенного места ядра. [38]
Спектроскопия ЯМР позволяет совершенно однозначно идентифицировать альдегиды. Под влиянием карбонильной группы альдегидный протон дезэкранируется сильнее, чем водород любых других группировок, за исключением атомов водорода, участвующих в образовании водородной связи. [39]
В отличие от аминов амиды кислот, несмотря на наличие в них остатка аммиака, не имеют основных свойств. Это обусловлено влиянием карбонильной группы, которая, обладая электроноакцеп-торным характером, оттягивает неподеленную пару электронов атома азота ( стр. [40]
В этой группе электронная плотность связи О - Н смещена к атому кислорода, имеющему большую электроотрицательность. В свою очередь под влиянием поляризованной карбонильной группы такое смещение усиливается еще в большей степени. [41]
Вследствие большого влияния карбонильной группы на непосредственно соединенный с ней гидроксил, связь О - Н в результате сольватирующего действия молекул воды легко разрывается; при этом образуется анион кислоты и ион гидроксония. С точки зрения электронной теории влияние карбонильной группы на состояние О - Н - связи объясняется, с одной стороны, тем, что она проявляет - / - эффект, а с другой, тем, что ее тс-электроны сопряжены с неподеленными электронными парами атома кислорода гидроксильнои группы ( - С-эффект); все это приводит к уменьшению дробного отрицательного заряда на кислороде гидроксильнои группы по сравнению с таковым в спиртах. [42]
Вследствие большого влияния карбонильной группы на непосредственно соединенный с ней гидроксил, связь О - Н в результате сольватирующего действия молекул воды легко разрывается; при этом образуется анион кислоты и ион гидроксония. С точки зрения электронной теории влияние карбонильной группы на состояние О - Н - связи объясняется, с одной стороны, тем, что она проявляет - / - эффект, а с другой, тем, что ее тс-электроны сопряжены с неподеленными электронными парами атома кислорода гидроксильной группы ( - С-эффект); все это приводит к уменьшению дробного отрицательного заряда на кислороде гидроксильной группы по сравнению с таковым в спиртах. [43]
Эти реакции протекают с альдегидами и кетонами, у которых атом углерода, непосредственно связанный с карбонильной группой, имеет хотя бы один атом водорода. Для понимания механизма реакции необходимо рассмотреть влияние карбонильной группы на алифатический радикал. Электроноакцепторная карбонильная группа вызывает поляризацию связей с соседними атомами, в частности связи С - Н у ос-атома углерода. За счет этого кислотного центра оксосоеди-нение может при действии сильных оснований отщеплять протон и превращаться в карбанион. Отрицательный заряд в образовавшемся карбанионе делокализован при участии альдегидной или кетонной группы. Анион представляет собой сильный нуклеофил и реагирует со второй молекулой карбонильного соединения по механизму нук-леофильного присоединения. [44]
Страницы: 1 2 3