Структура - заместитель
Cтраница 2
На примере алкилбензолов и нафтеноароматических углеводородов была показана независимость характера спектра от структуры заместителя. В связи с этим можно понять, почему спектры этилиндана, изопропил-индана, трет, бутилиндана, изобутилиндана и остальных замещенных инданов в положении 5 - имеют одно и то же распределение интенсивности в полосе и смещение положения максимумов поглощения в пределах всего 5 - 15 А. Прежде чем перейти к рассмотрению причин этого смещения максимумов поглощения на шкале длин волн, следует отметить отчетливую аналогию между спектрами 4 - и 5-метилинданов и метилбензолов соответствующего замещения, т.е. 1 2 3 - й 1 2 4-триметилбензолов. [16]
Шиманский [20] указывает на ряд ИК-частот моноалкилзамещенно-го бензольного кольца, нечувствительных к структуре заместителя. [17]
 |
Константы скорости образования гидропероксида при взаимодействии пероксидных радикалов с углеводородами 68 - 72 ]. [18] |
Проведенные квантовохимические расчеты показывают, что-дипольные моменты пероксидных радикалов сравнительно мало изменяются в зависимости от структуры заместителя. Все заместители R по отношению к пероксидной группе являются донорами электронов и увеличивают общий заряд на атомах кислорода. Неспаренный электрон находится на высшей занятой гс о-о - разрыхляющей молекулярной орбитали. Она образована двумя р-орбиталями атомов кислорода. [19]
Структура продуктов конденсации зависит от многих факторов, в том числе: функциональности силанола, структуры заместителей при атоме кремния, рН среды. Рассмотрим влияние этих факторов. [20]
Так как массовая эффективность пространственно затрудненных фенолов ( в отличие от мольной) слабо зависит от структуры заместителей и числа ОН-групп в молекуле ингибитора, то выбор конкретных алкилфенолов в качестве присадок к реактивным топливам определяется в основном технологическими и экономическими соображениями. [21]
 |
Термолиз монопероксикеталей КМеС ( ОМе ООСМе3 в алкилароматических углеводородах. [22] |
Термолиз монопероксикеталей [223] характеризуется параметрами, приведенными в табл. 5.22. Несмотря на значительное удаление от пер-оксидной группы, структура заместителя существенно влияет на кинетику термолиза, в частности, возможно невалентное взаимодействие кислородных атомов заместителя с пероксидной группой. [23]
В работе [113] также высказано предположение, что различие в токсичности производных меркаптобензотиазола определяется расположением атома азота в структуре заместителя. Если же атом азота не входит в состав цикла заместителя, то соединение оказывается малотоксичным. В таких случаях даже введение в молекулу второго цикла, как в случае Ы Ы - дициклогексил-2 - бензотиазол-сульфенамида, не приводит к увеличению токсичности соединения. [24]
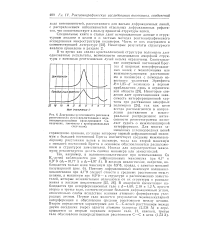 |
Диаграммы интенсивности рассеяния рентгеновских лучей циклогексаном и иоли-винилциклогексаном ( фильтрованное Си-излучение, гониометр с пропорциональным счетчиком. [25] |
Брегга соответствует среднему межмолекулярному расстоянию цепей в полимере, тогда как второй максимум с меньшей постоянной Eiperra в основном обусловливается расположением и структурой заместителей. Иногда для характеристики максимума рекомендуется делать снимки мономера или заместителей. [26]
Как отмечалось во введении, одним из существенных условий успешного использования радикалов в качестве спиновых зондов является постоянство значений их электронно-спиновых параметров, в частности, в зависимости от структуры заместителей у радикального фрагмента. [27]
Несмотря па существование целого ряда специализированных бактериолитических ферментов, действующих только на са-харидные или только па пептидные цепи ( см. табл. 30), было бы слишком большим упрощением полагать, что структура пептидных заместителей не влияет на эффективность действия гликоли-даз и, наоборот, что гидролиз пептидов не зависит от наличия сахар идных цепей в пептидогликане. Напротив, уже можно с определенностью заключить, что бактсриолитичсская активность и гликозидаз, и пептидаз определяется структурой пептидогликана в целом на достаточно большом удалении от потенциально расщепляемой связи в субстрате. Так, в работе [16] было показано, что если с помощью М - ацетилмурамоил - Ь - аланинамидазы ( КФ 3.5.1.28), не проявляющей карбогидразной активности, обработать пептидогликан бактериальной клеточной стенки и выделить чистый полисахарид, свободный от пептидных заместителей, то эффективность действия лизоцима по отношению к нему резко падает. Полученный полисахарид, который представлял собой чередующиеся остатки N-ацетилмурамовой кислоты и М - ацетилглюко-замина и имел среднюю степень полимеризации 20, плохо атаковался не только лизоцимом белка куриных яиц, но и всеми изученными лизоцимами бактериального происхождения. [28]
Можно отметить, что выход, как правило, растет с ростом числа углеродных атсмов в заместителях. Структура заместителей и их взаимное расположение на величину выхода, по-видимому, влияют слабо. [29]
Замена этих заместителей на - СНаОН и - СНг-О-СНз приводит к некоторому снижению эффекта ингибирования. Дальнейшее усложнение структуры заместителей в положении 4 приводит к еще более замет-кому снижению эффективности, что, по-видимому, связано с возрастанием стерических препятствий у феноксильных радикалов. [30]
Страницы: 1 2 3