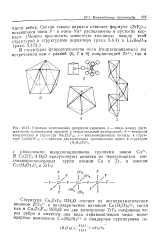
Структура - пирохлор
Cтраница 2
 |
Координация атомов А в структуре пирохлора А2В2Х6Х. [16] |
Тем не менее соотношение между граничной ( пока неизвестной) структурой, отвечающей случаю ( 1), и флюоритом представляет вполне определенный интерес, ибо некоторые соединения обнаруживают способность к переходу от структуры пирохлора к структуре дефектного флюорита. [17]
В результате высокотемпературного рентгенофазового анализа было установлено, что в случае Pb3NiNb209, Pb2FeNb06, PbsFe2W09, Pb2MgW06 и ряда других соединений интенсивное связывание РЬО начинается при 600 - г - - 700 С, причем первоначально образуется структура пирохлора, и лишь по мере увеличения температуры обжига становится заметным появление перовскита и исчезновение пирохлора. [18]
Согласно работе [ 2Д, в структуре пирохлора ионы занимают следующие позиции: 16 катионов типа А занимают позиции 16 ( С), 16 катионов типа В занимают позиции 16 ( О), 8 анионов - позишш 8 ( а), у минерала пирохлора эти позиции заняты ионами фтора. [19]
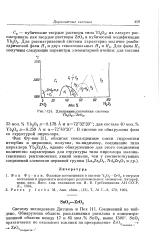 |
Диаграмма состояния системы Yb203 - Zr03. [20] |
В системе не обнаружена фаза со структурой пирохлора. [21]
Состав такого каркаса отвечает формуле оставшиеся ионы F и ионы Na расположены в пустотах каркаса. Можно проследить известную аналогию между этой структурой и структурами пирохлора ( разд. [23]
Близость координационных полиэдров Nd07 в окиси неодима и НЮ7 в моноклинной форме двуокиси гафния облегчает диффузию неодима в привычный для него кислородный координационный полиэдр двуокиси гафния и способствует непосредственному синтезу гафната неодима. А) приводит к неустойчивости моноклинного типа структуры в целом и превращению его в структуру пирохлора, характерную для гафната неодима. [24]
В только что описанных структурах взаимопроникающие сетки идентичны. Можно также указать структуры, состоящие из двух ( или большего числа) взаимопроникающих сеток, имеющих разное строение. В структуре пирохлора ( разд. Этот каркас ( рис. 7.4) оказывается устойчивым без участия седьмого атома О ( как в KSbOs) и может быть построен из октаэдров, расположенных тетраэдрически вокруг точек алмазной сетки, или же из октаэдров, помещенных на всех связях этой сетки. [25]
Ни в одной из работ не рассматривается, почему CdUNfUOr, столь сильно отличается по диэлектрическим свойствам от других аналогичных по составу представителей группы пирохлоров. Причина этого лежит, очевидно, в различиях атомного строения пирохлоров и перовскитов. Ниже дается описание особенностей структуры пирохлоров, проводится геометрический анализ ионных контактов в них, а в итоге дается кристаллохимический анализ условий возникновения спонтанной электрической поляризаши у веществ этого структурного типа. [26]
В работе [30] описан окисел состава U2 / 3Nb2O7, полученный при Г1400 С с кубической структурой типа пирохлора с параметром а 10 38 А. Однако рентгенограмма образца иМЬзОкн, резко охлажденного от температуры плавления 1520 С, показала только размытые линии той же фазы. Очевидно, состав окисла со структурой пирохлора определен неверно, но существование такой фазы в системе U - Nb - О представляется вполне вероятным. [27]
При диффузии неодима в тетрагональную двуокись циркония, происходящей также по вакансионному механизму, неодим входит в новый для него кислородный полиэдр Ме08, характерный как для тетрагональной, так и для кубической структуры. В результате этого образуется твердый раствор кубической структуры с неупорядоченным расположением катионов и вакансий в анионной подрешетке состава, соответствующего максимальному содержанию окиси неодима в кубических твердых растворах типа флюорита на равновесной диаграмме данной системы ( около 20 мол. Количество твердого раствора типа флюорита на первых стадиях процесса накапливается, образуя промежуточный продукт. И лишь в дальнейшем, при увеличении количества неодима в твердом растворе и упорядочении распределения вакансий и катионов, образуется цирконат неодима структуры пирохлора. [28]
А, образуя слегка искаженный куб, по в других случаях существует заметное различие между шестью расстояниями А-О и двумя другими расстояниями А-О. Остальные шесть атомов кислорода находятся на расстоянии 2 61 А. Эта особенность структуры пирохлора отмечена в гл. [29]
Пьезоэлектрические и пироэлектрические керамики применяют в электрических полях с высокой напряженностью. Большинство керамик подобных типов, наиболее широко используемых, представляют собой состав РЬ7гОз - РЬТЮз или основанные на нем многокомпонентные системы, такие как РЬ ( В1В) 2Оз - РЬТЮз. Недавно была синтезирована висмутсодержащая керамика со структурой перовскита, с малым содержанием свинца либо с его полным отсутствием состава Bio. Наличие структуры перовскита считают весьма важным для проявления пьезоэлектрических и пироэлектрических свойств подобных керамик. Это дает им существенные преимущества в сравнении с другими ферроэлектрическими оксидами, такими как вольфрамовые бронзы, структуры пирохлора или сложные висмутовые структуры. [30]
Страницы: 1 2 3