Структура - флюорит
Cтраница 1
Структуры флюорита и МгиО - Лили С - типа оксидов R j Q -, , где К - редкоземельные элементы) также очень близки. В связи с этим ( а также руководствуясь близостью ионных радиусов) ряд авторов экспериментально обнаружил в некоторых системах 1.2 3 - 2 2 3 - ТНОл и др. непрерывные ряды твердых растворов. С точки зрения, изложенной выше, при термодинамическом равновесии непрерывного ряда твердых растворов быть не может, так как процесс упорядочения кислородных вакансий с образованием фазы, имеющей структуру типа Ма о Ох с бтьемноцентрированной кубической ячейкой, параметр которой вдвое больше, чем у фазы с неупорядоченной структурой типа флюорита ( кубической гранецентрированной ячейкой), должен быть фазовым переходом первого рода. Действительно, все сверхструктурные узлы получаются из векторов группы 1 / 2 1 / 20 ( и эквивалентных им) и субструктурных узлов. [1]
Для структуры флюорита характерна одна формульная единица в кубической элементарной ячейке. Каждый ион металла окружен восемью анионами, а каждый анион в свою очередь - четырьмя ионами металлов, расположенными в вершинах тетраэдра. Фононная дисперсионная кривая имеет девять ветвей. [2]
В структуре флюорита CaF2 ( рис. 1.81) 8 ионов F, расположенных в вершинах куба, находятся в окружении 14 ионов Са2, 8 из которых занимают вершины и 6 - центры граней большого куба. [3]
В структуре флюорита ( рис. 6.9) атомы ( ионы) А окружены восемью атомами X по вершинам куба и атомы X - четырьмя атомами А по вершинам правильного тетраэдра. По этому типу кристаллизуются многочисленные дифториды и диоксиды ( табл. 6.3), некоторые дисилициды ( см. ниже), интерметаллические соединения ( например, GeMg2, SnMg2, PtAl2 и др.) и ди-гидриды переходных металлов. [4]
Меняя в структуре флюорита положения атомов металла и неметалла, получим антиизотипичную структуру антифлюорита. Кроме двойных, в структуре антифлюорита кристаллизуется большое число тройных соединений как с упорядоченным, так и со статистическим расположением атомов. MgSb ( Cu), MgBi ( Cu) [11], CdSb ( Cu) [12] элементы, которые в формуле стоят вне скобок, занимают позиции фтора вполне упорядочение, а элементы, стоящие в скобках, занимают позиции кальция. [5]
Меняя в структуре флюорита положения атомов металла и не - металла, получим антиизотипичную структуру антифлюорита. Кроме двойных, в структуре антифлюорита кристаллизуется большое число тройных соединений как с упорядоченным, так и со статистическим расположением атомов. Так, в LiMg ( N) [10] атомы Li и Mg распределяются статистически по позициям атомов фтора, в то время как в LiZn ( N) [10], AgMg ( As), MgSb ( Cu), MgBi ( Cu) [11], CdSb ( Cu) [12] элементы, которые в формуле стоят вне скобок, занимают позиции фтора вполне упорядо-ченн о, а элементы, стоящие в скобках, занимают позиции кальция. [6]
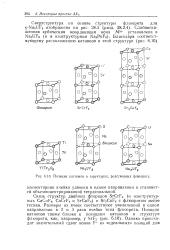 |
Позиции катионов в структурах, родственных флюориту. [7] |
Сверхструктура на основе структуры флюорита для Y - Na2UF6 изображена на рис. 28.3 ( разд. [8]
Фторид европия имеет структуру флюорита. [9]
Существует интересный пример деформации структуры флюорита, приводящей к образованию слабых взаимодействий металл - металл, который напоминает искаженные структуры рутилового типа для некоторых диоксидов. Атом металла окружен еще восемью соседними атомами Si по вершинам искаженного куба. Такое искажение структур типа флюорита можно рассматривать как частичный переход к структуре типа СиА12 ( разд. [10]
 |
Структура флюорита. [11] |
Позиции ионов Са2 в структуре флюорита соответствуют позициям кубической плотнейшей упаковки, позиции ионов F - - всем тетраэдрическим пустотам. [12]
Карбид бериллия имеет структуру антифлюорита [ структура флюорита ( рис. 43, стр. [13]
Автор показывает, как, изображая структуру флюорита и пирохлора в виде полиэдров, можно от первой структуры перейти ко второй. Однако нетрудно доказать, что здесь Ю. А. Пятенко допускает неточности. Во-первых, как будет показано ниже, у пирохлоров все восемь расстояний А-0 могут быть равны только при условии х 0 25, но у всех пирохлоров типа А2В207 х 0 25 и, следовательно, катионы типа А находятся внутри шестигранников, а не кубов. [14]
 |
Оксиды, оксофториды галогенов. [15] |
Страницы: 1 2 3 4