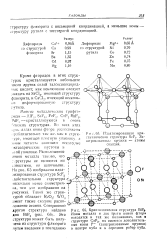
Структура - флюорит
Cтраница 4
Компоненты системы образуют твердые растворы на основе TuF3 с тисо-нптовон структурой и на основе SrF2 со структурой флюорита, между ними находи 1ся область смешанных фаз тисонита флюорита. [46]
По этой же причине соединение Pb2Nb3O7 кристаллизуется в искаженной ромбоэдрической структуре [27], тогда как Cd2NboO7 кристаллизуется в структуре флюорита с вакансиям. Такая ситуация, по-видимому, имеет место в случае кристаллов LioBi и p - Li3Sb [ 28J, где атомы Bi и Sb занимают позиции Са, а атомы Li - позиции F плюс позиции ( X) в центрах кубов. [47]
По этой же причине соединение Pb2Nb2O7 кристаллизуется в искаженной ромбоэдрической структуре [27], тогда как Cd Nb2O7 кристаллизуется в структуре флюорита с вакансиями в подрешетке из атомов О. Такая ситуация, по-видимому, имеет место в случае кристаллов Li3Bi и 3 - Li3Sb [ 281, где атомы Bi и Sb занимают позиции Са, а атомы Li - позиции F плюс позиции ( X) в центрах кубов. [48]
Она очень напоминает структуры многих соединений типа М АВа ] 2 или [ XYeP Z Две последние структуры - это структуры флюорита или антифлюорита ( см. рис. 4.1) с той лишь разницей, что анионы ( или катионы) представляют собой октаэдры, оси которых ориентированы параллельно граням куба. Соотношения двух структур можно установить на рис. 13.2, поскольку ионы Na обозначены здесь и светлыми кружками и кружками с крестиками. Если все кружки с Крестиками, один из которых находится в центре, а другие на ребрах, удалить, то структура криолита перейдет в структуру M. [49]
Фториды ZnF2, CdF2, HgF2 явл-яются более ионными соединениями, чем другие галогениды, и кристаллизуются в основном в структуре флюорита. Фториды - труднорастворимые вещества, менее растворимые, чем другие галогениды; относительная растворимость в ряду ZnF2 - CdF2 - HgF возрастает. Это связано не только с высокой энергией решетки фторидов, но и с тем, что для фторидов, в отличие от прочих гало-генидов, не характерно образование фторидных комплексов. [50]
Окислы, сульфиды, селе-ниды и теллуриды лития, натрия и калия кристаллизуются в антафлюоршпной структуре, геометрически идентичной со структурой флюорита, но с взаимно измененным положением положительных и отрицательных ионов. Перечень фторидов и окисло. [51]
Кроме фторидов в этих структурах кристаллизуется небольшое число других солей галоидоводород-ных кислот; как исключение следует указать на SrCl2, имеющий структуру флюорита, и СаС1, имеющий несколько деформированную структуру рутила. [53]
В этой структуре ( рис. 10.5) ионы К1 и PtCl62 - занимают соответственно положения ионов F - и Са2 в структуре флюорита. В противоположность структурным типам I GeFe и K2MnF6, которые в значительной степени ограничены лишь структурами фторидов, в структурном типе K2PtCl6 ломимо гексафторидов кристаллизуются также гексахлориды, гексабро-миды и некоторые гексаиодиды тяжелых щелочных металлов ( например, Rb2SnI6l Cs2TeI6), аммония и таллия. Для некоторых гексабромидов и гек-саиодидов реализуется менее симметричный вариант этого структурного типа. [54]
 |
Кристаллические структуры тенорита СиО и AgO ( a, a также PdO. [55] |
Оксиды МО-2 - Большинство диоксидов кристаллизуются в одном из двух простых структурных типов: наиболее крупные ионы М4 имеют координационное число 8 в структуре флюорита, а менее крупные - координационное число 6 в структуре рутила. Термин структурный тип рутила в табл. 12.4 подразумевает как наиболее симметричную ( тетрагональную) разновидность этой структуры, так и менее симметричные варианты, причем последние выделены в таблице штриховыми линиями. Для этих соединений характерен полиморфизм, например РЬС2 и ReO2 кристаллизуются также в структурном типе а - РЬО2 ( разд. [56]
Страницы: 1 2 3 4