Структура - флюорит
Cтраница 3
Диоксид СеОз образуется при непосредственном взаимодействии компонентов и кристаллизуется в структуре флюорита. Он плавится при 2600 С под давлением кислорода, начинает отщеплять кислород только при 2300 С. При 1250 С СеО2 восстанавливается водородом до Се2Оз - Диоксид церия не растворяется в воде, а после прокаливания - и в кислотах, и в щелочах. [31]
Диоксид СеО2 образуется при непосредственном взаимодействии компонентов и кристаллизуется в структуре флюорита. Он плавится при 2600 С под давлением кислорода, начинает отщеплять кислород только при 2300 С. При 1250 С Се02 восстанавливается водородом до Се20з - Диоксид церия не растворяется в воде, а после прокаливания - и в кислотах, и в щелочах. [32]
Для ионных соединений типа АХ, известны две простые структуры: структура флюорита и структура рутила. В структуре флюорита ионы металла окружены восемью, а в структуре рутила - шестью отрицательными ионами. Многие двуокиси и дифториды имеют подобные структуры. [33]
Кристаллическая структура галогенидов лития напоминает структуру хлорида натрия, а не структуру флюорита, характерную для галогенидов щелочноземельных металлов. Тем не менее свойства галогенидов лнтия позволяют предполагать близкое сходство лития с щелочноземельными элементами. [34]
Хг кристаллизуется таким же образом, оно, как говорят, имеет структуру флюорита; если соединение типа MJX2 кристаллизуется аналогичным образом, но с ионами Х2, занимающими положение Са2, и ионами М, занимающими положение F, то говорят, что оно имеет антифлюоритовую структуру. Вторую структуру, которую часто обнаруживают у соединений состава 1: 2 ( структура минерала рутила Ti62), называют структурой рутила; она показана на рис. 2.7. Некоторые соединения типа MJX2 кристаллизуются с образованием антирутиловой структуры. [35]
Фторид ртути ( П) является по существу ионным и кристаллизуется в структуре флюорита. Он почти полностью разрушается даже холодной водой, что естественно для ионных солей, образованных слабой кислотой и чрезвычайно слабым основанием. Ртуть ( П) не только не проявляет тенденции к образованию ковалентной связи Hg-F, но не образует и фторидных комплексов. [36]
Фторид ртути ( II) является по существу ионным и кристаллизуется в структуре флюорита. Он почти полностью разрушается даже холодной водой, что естественно для ионных солей, образованных слабой кислотой и чрезвычайно слабым основанием. Ртуть ( П) не только не проявляет тенденции к образованию ковалентной связи Hg-F, но не образует и фторидных комплексов. [37]
Компоненты системы образуют дважды ограниченные твердые растворы на основе компонентов: со структурой флюорита - на основе BaF2, со структурой тисонита-на основе ErF3 и смешанную область тисонита флюорита. [38]
Компоненты системы образуют ограниченные твердые растворы: на основе BaF2 - со структурой флюорита, на основе YbF3 - со структурой тнсонита и смешанную область фаз тиоонита флюорита. [39]
Было получено лишь несколько твердых соединений, в частности желтая окись BkO2, имеющая структуру флюорита. [40]
Компоненты системы образуют дважды ограниченные твердые растворы на основе компонентов: SrFz - со структурой флюорита и LaF3 - со структурой тисонита, между которыми находится смешанная область тисонита флюорита. [41]
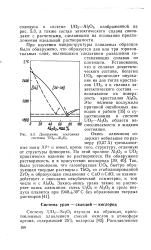 |
Диаграмма состояния Окись алюминия СО. [42] |
А) трехвалентные ионы А13 и имеет, кроме того, структуру, отличную от структуры флюорита. По этой причине А12О3 и 1Ю2 практически взаимно не растворяются. [43]
Присутствие окиси гадолиния в области флюорит-ного твердого раствора и аномальное поведение параметра решетки объясняются переходом структуры флюорита с идеальной анионной решеткой к структуре с вакансиями. [44]
Нами [31] с использованием этой модели были рассчитаны зависимости энергий взаимодействия дефектов от состава фазы со структурой флюорита ( Evv и Еее), зависимости А 50г () оксидов МО2 - д; с этой структурой ( а 5 4 А) и разными значениями / С [ 25, 35, 65, 851 при 1000 К. [45]
Страницы: 1 2 3 4