Структура - боковая цепь
Cтраница 2
Сельер и Кеньон [19], сравнивая вычисленную и измеренную температуры плавления сополимеров этилена и винилового спирта, пришли к заключению, что фрагменты винилового спирта образуют кристаллическую решетку, причем структура боковых цепей сильно влияет на процесс кристаллизации. На свойства сополимеров этилена и винилового спирта решающее влияние оказывает не только способность к кристаллизации, но и межмолекулярные когезионные силы, обусловленные образованием мостико-вых водородных связей. В то время как этилен-винилацетатные сополимеры с повышением доли сомономера становятся мягче и эластичнее, у омыленного сополимера с увеличением содержания ОН-групп растут твердость и жесткость. [17]
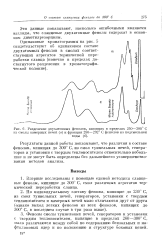 |
Разделение двухатомных фенолов, кипящих в пределах 260 - 300 С из смолы камерных печей ( о и фракции 290 - 292 С фенолов из подсмольной. [18] |
Фенолы смолы туннельных печей, генераторов и установки с твердым теплоносителем, кипящие в пределах 260 - 300 С, мало различаются между собой по содержанию бензольных и нафталиновых ядер и по положению и структуре боковых цепей. [19]
Возможности газохроматографического определения группового состава ограничиваются свойствами адсорбентов и стационарных жидких фаз, которые должны обладать максимальной селективностью по таким структурным элементам, как бензольное или нафтеновое кольца, при минимальной разделяющей способности по числу, положению и структуре боковых цепей. [20]
Однако, несмотря на большие преимущества, открываемые применением модифицированных бентонов и жидких кристаллов в случае анализа ксилолов, диэтилбензолов, некоторых других ароматических углеводородов и их производных, разработанные методики являются мало пригодными для анализа углеводородов, изомерных по структуре боковой цепи. Вследствие небольшой эффективности ( в сравнении с капил - лярными колонками) насадочные колонки не обеспечивают удовлетворительного разделения широкого спектра ароматических углеводородов С ] 0 - Сц при использовании любой из известных неподвижных фаз. [21]
В приведенной таблице указывается, как правило, только один какой-нибудь вид, у которого обнаружено то или иное соединение, хотя некоторые из них встречаются у нескольких видов растений. Что касается структуры боковой цепи, то эти соединения являются в основном производными 1 - или 2-пропена. Полагают, что кониферин ( I) ( фиг. [22]
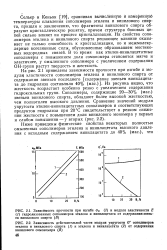
Однако структура и распределение боковых цепей изучены пока еще очень плохо. Единственным методом, позволяющим получить некоторое представление о структуре боковых цепей и их количестве в молекулах масляных углеводородов, является исследование спектров поглощения этих углеводородов в инфракрасной части спектра. [23]
Видно, что миграция заместителей может протекать как с небольшим поглощением, так и с небольшим выделением тепла в зависимости от их начальной ориентации. Изомеризация алкил-циклопентанбв и алкилцйклогексанов с уменьшением числа заместителей за счет изменения структуры боковых цепей идет с небольшим поглощением тепла и невысокими константами равновесия, практически одинаковыми для углеводородов этих двух групп. [24]
Так, например, УФ-спектр указывает на тип ароматической системы пли сопряженной поглощающей группы; ИК-спектр позволяет обнаружить наличие многих функциональных групп; спектр ЯМР дает в ряде случаев информацию об окружении этих групп. Кроме того, по данным масс-спектра можно сделать вывод относительно размера и структуры боковых цепей; прямое определение молекулярного веса дает значения с точностью до одной единицы массы. [25]
Однако, как правило, боковые цепи ароматических углеводородов масляных фракций значительно короче, чем боковые цепи соответствующих им по температуре выкипания нафтеновых углеводородов. Одним из важнейших вопросов в исследовании строения молекул ароматических углеводородов является определение числа и структуры боковых цепей. Наиболее точным методом, позволяющим получить представление об этом, является метод спектрального анализа в инфракрасной части спектра. [26]
Поскольку молекулярные веса белков варьируют в широких пределах, такого рода формулы не совсем пригодны для сравнения соотношений различных аминокислот в белковой молекуле. Надо, однако, указать, что именно эти соотношения определяют физические и химические свойства белков, поскольку последние зависят главным образом от структуры боковых цепей R в пептидных группировках. [27]
Пепсин действует преимущественно на внутренние пептидные связи, довольно далеко расположенные от концов полипептидной цепи, так как среди продуктов пепти-ческого гидролиза белка находят значительное количество полипептидов. Однако под влиянием пепсина разрываются также и некоторые пептидные связи, находящиеся на конце полипептидной цепи. Структура боковых цепей или радикалов аминокислот, находящихся по соседству от пептидной связи, определяет ее. Представление о том, что гидролитический распад белка под влиянием пепсина не сопровождается появлением свободных аминокислот, в настоящее время должно быть отвергнуто. Так, при помощи нингидринового метода, позволяющего определять наличие свободных аминокислот, было показано, что гидролиз фибрина кристаллическим пепсином сопровождается выделением заметного количества свободных аминокислот. Доказано, что пепсин наиболее быстро расщепляет пептидные связи, образованные аминогруппами ароматических аминокислот, а также связи ала-ала и ала-сер и ряд других. [28]
Продукты деградации алкалоидов часто представляют собой гетероароматические кольца, к которым присоединены различные боковые цепи; структура этих боковых цепей нередко позволяет раскрыть особенности строения исходной молекулы. Иногда величину и структуру боковой цепи значительно легче определить масс-спектрометрически, чем с помощью химической деградации. Тип присутствующей ароматической системы легко установить по ультрафиолетовому спектру, но часто его можно выяснить также и с помощью масс-спектра. [29]
Структура ди - и триалкилтетрагидрофуранов, получающихся при гидрировании 1-фурилалканолов - З в паровой фазе, подтверждает механизм реакции, данный выше: сначала происходит гидрогенолиз фуранового цикла, а затем образовавшийся 1 4-алкандиол в результате внутримолекулярного отщепления воды превращается в соответствующий тетрагидро-фуран. Это обстоятельство открывает широкие возможности синтеза различных гомологов тетрагидрофурана, так как структура боковой цепи 1-фурилалканолов - З, определяющая структуру вновь образующегося замещенного тетрагидрофуранового кольца, может изменяться в зависимости как от строения карбонилсодержащей группы в фурановом соединении, так и от строения алифатического кетона. [30]
Страницы: 1 2 3