Пористая структура - силикагель
Cтраница 1
Пористая структура силикагеля, как и других гелеобразных адсорбентов, формируется также и в процессе сушки. Объем геля при сушке уменьшается в десять и больше раз. [1]
Поскольку пористая структура жестких силикагелей при смене элюентов не меняется, то не наблюдаются и изменения селективности разделительной системы, если только геометрия растворенных полимерных молекул не зависит от вида растворителя. [2]
Изучение пористой структуры силикагелей О, 2 и 5, полученных из концентрированных водных золей кремнекислоты ( КВЗК) [4], приготовленных по [5], показало, что характер взаимосвязи между основными параметрами их пористой структуры носит иной характер, чем у силикагелей эталонного ряда. В таблице приведены данные, характеризующие пористую структуру силикагелей О, 2 и 5, из которой видно, что они являются однороднопереходнопористыми адсорбентами с незначительным объемом микропор. [3]
Изучение пористой структуры силикагелей О, 2 и 5, полученных из концентрированных водных золей кремнекислом ( КВЗК) [4], приготовленных по [5], показало, что характер взаимосвязи между основными параметрами их пористой структуры носит иной характер, чем у силикагелей эталонного ряда. В таблице приведены данные, характеризующие пористую структуру силикагелей О, 2 и 5, из которой видно, что они являются однороднопереходнопористыми адсорбентами с незначительным объемом микропор. [4]
Перечисленные пути регулировки пористой структуры силикагеля позволяют изменить удельную поверхность при одновременном изменении пористости или получать адсорбенты с одинаковой удельной поверхностью, но разными объемом и радиусом пор. [5]
Перечисленные пути регулирования пористой структуры силикагелей позволяют также получать образцы с одинаковой удельной поверхностью, но с разным сорбционным объемом пор и, наоборот, с разными величинами удельной поверхности, но с одинаковым объемом пор. [6]
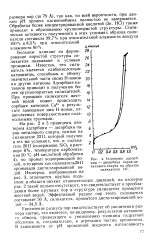 |
Изотермы адсорбции - десорбции паров метилового спирта на образце силикагеля 141. [7] |
Большое влияние на формирование пористой структуры силикагеля оказывают и условия промывки. Известно, что сили-кагель является слабокислотным катионитом, способным к обмену значительной части своих Н - ионов на другие катионы. Адсорбция катионов приводит к получению более крупнопористых силикагелей. При промывке силикагеля жесткой водой может происходить сорбция катионов Са2 1 в результате замещения ими Н - ионов, отщепляемых поверхностными сила-нольными группами. [8]
Для понимания механизма формирования пористой структуры силикагелей необходимо иметь ясное представление о генезисе силикагеля и его строении. В следующей главе рассмотрены эти вопросы. [9]
Кинетика сорбции протактиния определяется пористой структурой силикагеля. В случае использования крупнопористого силикагеля равновесие устанавливается менее чем за 3 часа ( 22 С), в то время как для мелкопористого силикагеля оно не достигается и за 8 час. Влияние температуры на сорбцию протактиния незначительно. Температуру 20 - 30 С следует считать оптимальной. Протактиний количественно поглощается из 6 М HN03 в колонке силикагеля ( длиной 10 см, диаметром 0 5 см) и не вымывается при пропускании через нее объема 6 М раствора HN03, равного 100 объемам колонки. [10]
Одним из возможных путей регулирования пористой структуры силикагелей является путь, основанный на использовании в качестве исходного сырья концентрированных золей кремневой кислоты, размер коллоидных частиц, которых поддается регулированию в процессе получения золя. Согласно [219] вначале получают разбавленный золь со значением рН 3 0 пропусканием раствора жидкого стекла через катионитв водородной форме и доводят рН золя до 7 3 введением в него щелочи. Один объем щелочного золя кипятят определенное время, после чего добавляют к нему второй объем холодного щелочного золя-питателя при продолжающемся кипячении всей массы золя в сосуде. При этом полагают, что на первой стадии при кипячении золя происходит поликонденсация первичных относительно мелких частиц и увеличение их размеров; на второй стадии - дальнейший рост частиц происходит уже в основном за счет конденсации добавляемых поликремниевых кислот из холодного золя-питателя на образовавшихся в первой стадии ядрах конденсации. Студни, приготовленные выпариванием водных золей, сушат при температуре 80 - 100 и затем 180 - 200 С. [11]
Как влияют условия получения на параметры пористой структуры силикагеля. [12]
Литературные сведения о влиянии последних на пористую структуру силикагеля весьма скудны и носят отрывочный характер. Авторы с сотрудниками попытались восполнить пробел в данном вопросе постановкой специальных исследований, результаты которых являются содержанием данного раздела. [13]
В предыдущих главах были рассмотрены пути регулировки пористой структуры силикагеля, основанные на изменении рН гелеобразования, последующей обработки гидрогеля перед сушкой и условий старения. Между тем пористая структура силикагеля зависит также от способа получения золя и превращения его в студень или коагель. При этом имеется в виду природа взаимодействующих растворов кремнесодержащего соединения и коагулятора, среда, в которой происходит процесс застудневания, и др. В данной главе показано, как влияют некоторые из перечисленных факторов на пористую структуру силикагеля. [14]
При этом показано, что механизм формирования пористой структуры силикагелей может быть распространен в основных чертах и на смешанные сорбенты, полученные совместным осаждением. Однако здесь следует учитывать влияние на процесс формирования второго компонента смеси, в частности те химические явления, которые разыгрываются на поверхности мицелл гидрогеля. Установлено, что факторы, влияющие на конечную пористую структуру силикагеля, влияют аналогичным образом и на структуру смешанных сорбентов. Конечная структура смешанного сорбента, один из компонентов которого вводится в золь в виде твердой высокодисперсной фазы с заданной пористой структурой, будет зависеть, с одной стороны, от его химического состава и, с другой - от природы добавляемого порошка и золя. Часто смешанный адсорбент приобретает новые свойства, делающие его весьма ценным поглотителем, носителем каталитически активных веществ и катализатором химических реакций. [15]
Страницы: 1 2 3 4