Изменение - скачок - потенциал
Cтраница 2
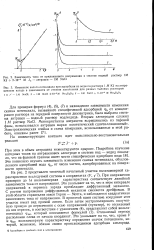
Из уравнения ( 114 4) непосредственно видно, что величина и даже знак изменения скачка потенциала в двойном слое определяются наряду с изменением WQ также изменением / пр вдоль поверхности электрода. Если размешивание вызвано собственным движением поверхности электрода под действием неравномерной поляризации, то между поведением поверхности ртути при ее положительном и при отрицательном заряде будет существенное различие. При таком допущении участок 1 модели соответствует нижней, легче поляризуемой части капельного электрода, участок 2 - его верхней части. [16]
Влияние строения двойного слоя на необратимые полярографические волны в общем случае обусловлено тремя основными факторами: изменениями эффективного скачка потенциала между электродом и разряжающейся частицей, концентрации ионов у электродной поверхности по сравнению с объемом раствора и ад-сорбируемости веществ. [17]
Влияние строения двойного слоя на необратимые полярографические волны в общем случае обусловлено тремя основными факторами: изменениями эффективного скачка потенциала между электродом и разряжающейся частицей, концентрации ионов у электродной поверхности но сравнению с объемом раствора и адсорбируемое веществ. [18]
Влияние строения двойного слоя в случае электродных процессов с участием органических веществ проявляется главным образом в изменении эффективного скачка потенциала между электродом и реагирующей на нем частицей, в изменении концентрации заряженных частиц в приэлектродном слое по сравнению с ее величиной в глубине раствора ( в частности, в изменении рН), а также в изменении адсорбируемости частиц на поверхности электрода. Двойной слой оказывает влияние на скорость переноса электронов, поэтому влияние строения двойного слоя проявляется лишь в случае электродных процессов с необратимой электрохимической стадией. [19]
Существуют по крайней мере три механизма влияния электролита фона на адсорбцию органических веществ: во-первых, через изменение скачка потенциала в диффузном слое, во-вторых, через эффект высаливания и, в-третьих, через специфическую адсорбцию анионов фона. [20]
Для проверки формул ( 4), ( 5), ( 7) и нахождения зависимости изменения скачка потенциала, вызванного специфической адсорбцией фа от концентрации раствора на передней поверхности диэлектрика, была выбрана система антрацен - водный раствор иод / иодида. [22]
При потенциометрическом титровании эквивалентная точка определяется не по изменению цвета индикатора, как это делается при обыкновенном объемном методе титрования, а по изменению скачка потенциала электрода. [23]
В простейшем случае - необратимой электрохимической реакции восстановления без участия ионов водорода в потенциал-определяющей стадии - изменение потенциала полуволны при изменении строения двойного слоя определяется изменением эффективного скачка потенциала между электродом и реагирующей частицей. [24]
Сущность метода состоит в том, что эквивалентная точка определяется не по изменению цвета индикатора, как это делается при обыкновенном объемном методе титрования, а по изменению скачка потенциала электрода. [25]
Необходимо отметить, что строгий количественный учет влияния растворителей на ЕЧ, [ по уравнениям типа ( 126), ( 127) или др. ] невозможен, так как неизвестно изменение скачка потенциала жидкостного соединения при изменении природы растворителя и сохранении неизменным растворителя в электроде сравнения. [26]
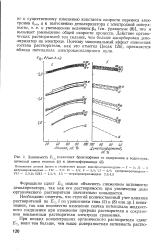 |
Зависимость Ег различных бромтиофенов от содержания в водно-орга. нической смеси этанола ( а и диметилформамида ( б. [27] |
Необходимо отметить, что строгий количественный учет влияния растворителей на Ег 2 [ по уравнениям типа ( 2) и ( 8) или др. ] невозможен, так как неизвестно изменение скачка потенциала жидкостного соединения при изменении природы растворителя и сохранении неизменным растворителя электрода сравнения. [28]
Необходимо отметить, что строгий количественный учет влияния растворителей на ЕЧ, [ по уравнениям типа ( 126), ( 127) или др. ] невозможен, так как неизвестно изменение скачка потенциала жидкостного соединения при изменении природы растворителя и сохранении неизменным растворителя в электроде сравнения. [29]
Поскольку поверхность ртути в электроде сравнения в несколько тысяч раз больше поверхности ртути в капилляре, сопротивление раствора невелико, а сила поляризующего тока ничтожна, то можно считать, что все изменение подаваемого напряжения приходится на изменение скачка потенциала на поверхности ртути в капилТгяре, так как потенциал электрода сравнения, благодаря чрезвычайно малой плотности тока на нем, будет практически постоянным. [30]
Страницы: 1 2 3 4