Электронное влияние
Cтраница 1
Электронные влияния на гидролиз заместителей в иных положениях, чем у С-2, значительно слабее. [1]
Электронное влияние пара-заместителя на характер делокали-зации неспаренного электрона отражается и на спектральных характеристиках феноксильных радикалов 9 - 4в67 - 82 8386 - 89 - эт-юв В ЯК-спектрах8 9 82 83 97 - 100 104 - 108 большинства феноксильных радикалов имеется дублетная полоса в области 1570 - 1670 см-1, близкая к частоте колебаний сопряженной карбонильной группы. [2]
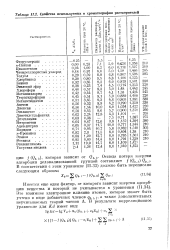 |
Свойства используемых в хроматографии растворителей. [3] |
Это взаимное электронное влияние атомов, которое может быть учтено в виде добавочных членов д0, у, а также дополнительных неучитываемых теорий членов А. [4]
Если электронные влияния различных алкильных групп примерно одинаковы, возрастание стерических препятствий в ряду ( 6 - 20) должно вызывать все возрастающие помехи сольватации. Это может быть причиной, почему влияние различных - алкильных заместителей следует порядку Бекера - Натана. [5]
Кроме электронного влияния, передаваемого в основном по линии ковалентных связей, заместитель может оказывать влияние на константы ионизации органических кислот при введении объемистых заместителей, особенно на близком расстоянии от карбоксильной группы, так как эти заместители будут создавать препятствия для сольватации как кислоты, так и в большей степени соответствующего аниона. Это должно, дестабилизировать конечное состояние больше, чем исходное. [6]
Передачу электронного влияния он объясняет индукционным эффектом и л л-сопряжением колец. Из таблицы 3 можно видеть снижение передачи электронных влияний в производных бифенила, где увеличена акопла-парность бензольных ядер. [7]
Для описания электронного влияния СН2 - группы на положение характеристического симметричного колебания ( 2908 - 2817 см-1) СНз-заместителя в карбанионе необходимо найти зависимость между VCH и параметрами электронного строения метил замещенных молекул. [8]
Для разделения общего электронного влияния на мезомерную и индукционную составляющую необходимо знать индукционную константу GJ. [9]
Аналогично могут передавать электронное влияние и ароматические системы. [10]
Если не преобладает электронное влияние, то замещение в орто-поло-жение может оказаться затрудненным пространственными эффектами уже присутствующего заместителя при увеличении его объема. Это показывают данные по нитрованию алкилбензолов. [11]
Аналогично могут передавать электронное влияние и ароматические системы. [12]
Во-первых, если электронное влияние лигандов через центральный атом будет не особенно велико - порядка сотых долей CM-Z при характеристике влияния недиагональными силовыми постоянными - то колебания каждого лиганда будут проявляться в спектре независимо от других лигандов. Результирующий наблюдаемый спектр образуется как аддитивная сумма спектров отдельных лигандов, расположенных вокруг центрального атома. Если эти лиганды одинаковы, то появится большое число случайно вырожденных частот. Это обстоятельство, в свою очередь, отразится на значениях интенсивностей результирующих полос поглощения, которые не будут подчиняться обычному для ИК-спектро-скопии векторному правилу сложения векторов изменений дипольных моментов лигандов при колебаниях, а будут складываться алгебраически. Кроме того, это отразится и на поляризациях наблюдаемых колебаний, что необходимо принимать во внимание при поляризационных измерениях в кристаллах. [13]
Оксидная группа оказывает двойственное электронное влияние. С одной стороны, она действует как сильный резонансный донор электронов за счет отрицательно заряженного атома О, а с другой - как сильный индуктивный акцептор электронов за счет положительно заряженного атома N. Именно благодаря донорному эффекту N-оксидной группы значительно увеличивается электронная плотность на Сз по сравнению с С4, и на нем наводится отрицательный заряд. [14]
Оксидная группа оказывает двойственное электронное влияние. С одной стороны, она действует как сильный резонансный донор электронов за счет отрицательно заряженного атома О, а с другой - как сильный индуктивный акцептор электронов за счет положительно заряженного атома N, Именно благодаря донорному эффекту N-оксидной группы значительно увеличивается электронная плотность на С3 по сравнению с Сд, и на нем наводится отрицательный заряд. [15]
Страницы: 1 2 3