Четвертичная структура - белок
Cтраница 3
У ряда белковых соединений несколько сложных полипептидных цепей белка могут агрегироваться вместе, создавая более сложный комплекс определенного строения, называемый четвертичной структурой белка. Каждая полипептидная цепь, образующая четвертичную структуру, называется субъединицей и сохраняет свойственные ей первичную, вторичную и третичную структуры, однако биологическая роль комплекса в целом отличается от биологической роли субъединиц вне комплекса. Фиксация четвертичной структуры обеспечивается водородными связями и гидрофобными взаимодействиями между субъединицами. Например, молекула гемоглобина - белка с четвертичной структурой - состоит из четырех субъединиц, окружающих гем ( простетическую железосодержащую группу - железопорфирин); между субъединицами нет кова-лентной связи, однако тетрамер представляет собой единое целое, в котором субъединицы тесно связаны и ведут себя в растворе как одна молекула. Наличие четвертичной структуры характерно также для других металлопротеинов и для иммуноглобулинов. При формировании четвертичной структуры белка образующийся комплекс может содержать, помимо субъединиц полипептидной структуры, и субъединицы иной полимерной природы, а также соединения других классов. [31]
Миоглсбины млекопитающих обнаруживают лишь очень незначительный эффект Бора, поэтому до последнего времени полагали, что эффект Бора обязательно сопряжен с изменениями четвертичной структуры белка, как, например, в тетрамерных гемоглобинах млекопитающих. Однако недавно хорошо выраженный эффект Бора был обнаружен у двух мономерных гемоглобинов Chir-onotnus. Таким образом, гетеротропное взаимодействие мсжет быть сопряжено с изменениями только третичной структуры или с изменениями третичной и четвертичной структур однонременко. [32]
Это позволило отделить индуцированные лигандами изменения третичной структуры субъединиц от изменений третичной структуры, которые, как предполагается, возникают вследствие изменений четвертичной структуры белка. К сожалению, модифицирующий реагент ( БМЭ) препятствовал также и свободному движению тирозинового остатка НС2 в fl - цепи, поэтому определенные выводы удалось сделать только относительно изменений в 3-цепях. [33]
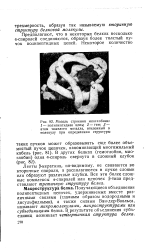 |
Модель строения миоглобина. 1 - полипептидная цепь. 2 - гем. 3 - атом тяжелого металла, введенный в молекулу при определении структуры. [34] |
Получающиеся объединения полипептидных цепочек, удерживаемых вместе различными связями ( главным образом водородными и дисульфидными), а также силами Ван-дер - Ваальса, называют макромолекулами, микроструктурами или субъединицами белка, результате объединения субъединиц возникает четвертичная структура белка. [35]
Различают первичную, вторичную, третичную и четвертичную структуру белка. [36]
Эта модель объясняет многие особенности дифракционной картины как на кубических, так и на тетрагональных кристаллах и их векторные карты Паттерсона. Для точного определения четвертичной структуры белка необходим более детальный анализ кристаллической структуры, который в настоящее время пытаются осуществить. Полное понимание функций белка всецело зависит от знания тонких особенностей его структуры, но даже не зная их, очень многое можво понять о природе железного ядра, его связи с белком и биосинтезе молекулы ферритина. Для последующего обсуждения необходимо лишь знать, что белковая оболочка представляет собой правильный ансамбль из субъединиц, охватывающий железосодержащее ядро и позволяющий железу входить и выходить из молекулы по каналу между субъединицам. [37]
В книге подробно рассматриваются автоматический метод анализа пептидов и белков с помощью ионообменной хроматографии, газожидкостная хроматография аминокислот и пептидов, очистка белков с помощью гель-фильтрации и электрофореза, изучение функциональных групп в белках с привлечением химических методов. Отдельная глава посвящена изучению четвертичной структуры белков. [38]
Величина lg / С координации кислорода с Fe ( II) в гемоглобинах и миоглобинах может изменяться на 4 5 и более за счет искажения структуры комплексов Fe ( II) и FeHO2, а также за счет комплементарных ( или кооперативных) изменений конфигурации полипептида. Кроме того, изменения четвертичной структуры белка сами по себе могут привести к изменению lg / С на 2 5 единицы ( разд. [39]
Да и сама классификация - первичная, вторичная, третичная, четвертичная структура белка - обоснована Берналом. [40]
Да и сама классификация - ( первичная, вторичная, третичная, четвертичная структура белка - обоснована Берналом. [41]
Многие белки состоят из субъединиц, одинаковых или различных, образующих трехмерные ассоциаты или более сложные ансамбли. В этом случае принято говорить о четвертичной структуре белков. Специфичность четвертичной структуры данного белка обусловливается выполняемой им биологической функцией, а взаимодействие субъединиц обеспечивает дополнительный механизм ее регуляции. [42]
 |
Схема антипараллельной цепной структуры белка, обнаруженной в волокнах шелка. [43] |
Рентгеноструктурное изучение гемоглобина ( выполненное английским ученым Максом Перутцем с сотрудниками) показало, что молекула этого белка представляет собой агрегат из четырех субъединиц, каждая из которых напоминает молекулу миоглобина и содержит одну полипептидную цепь. Такое сочетание двух или большего числа полипептидных цепей называют четвертичной структурой белка. [44]
Страницы: 1 2 3 4
