Сублимация - металл
Cтраница 2
Однако в реальных условиях ( твердое состояние металла и продукта его окисления, молекулярное состояние окислителя) реакция осложняется процессами сублимации металла, диссоциации молекул окислителя и кристаллизации продукта окисления. [16]
Поскольку поправка на электроотрицательность относительно невелика, из уравнения (VII.2) следует ожидать линейную зависимость между энергией связи QM-H и теплотой сублимации металла. [17]
Все величины, стоящие в правой части уравнения, можно определить экспериментально. Теплота сублимации металла определяется для некоторых элементов прямыми калориметрическими измерениями или на основании изменения давления сублимации с температурой. Энергия диссоциации ( например молекул галогенов) вычисляется по величинам констант диссоциации при различных температурах или некоторыми оптическими способами. Энергия ионизации металлических атомов может быть найдена по методу бомбардировки электронами или с помощью более точных спектральных способов. Так, например, эти величины были найдены из предельных частот главных серий паров металлов. [18]
Устойчивость соединений с высшими степенями окисления увеличивается в порядке 3d С 4d 5d, что является, вероятно, следствием действия по крайней мере двух факторов. Во-первых, энергия сублимации металла увеличивается в группе с ростом атомного номера элемента, что требует для ее компенсации либо упрочения, либо образования большего числа связей. Во-вторых, возможность формирования очень прочной ковалентной связи, усиленной за счет способности ( п - 1) d - орбиталей к образованию я-связи ( в данном случае я-акцепторной способности с лигандами типа F - и О2 -), по-видимому, растет, а не уменьшается при переходе вниз по группе. Таким образом, смещение ст - и п-электронов от лигандов к центральному атому металла усиливается при увеличении эффективного заряда ядра вниз по группе. [19]
При, этом еле -, дует учесть работу выхода электрона для ртути и данного металла, а также теплоту сублимации атома металла из его решетки и из амальгамы. Данных по теплотам сублимации металлов из их амальгам очень мало, а поэтому необходимо провести экспериментальные исследования в этом направлении. [20]
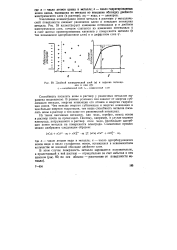 |
Двойной электрический слой ( а и падение потенциала в нем ( б. [21] |
Способность посылать ионы в раствор у различных металлов выражена неодинаково. В равных условиях она зависит от энергии сублимации металла, энергии ионизации его атомов и энергии гидратации ионов. Чем меньше энергия сублимации и энергия ионизации и чем больше энергия гидратации, тем выше способность металла посылать ионы в раствор и тем ниже его равновесный потенциал. [22]
Способность посылать ионы в раствор у различных металлов выражена неодинаково. При одинаковых условиях она зависит от энергии сублимации металла, энергии ионизации его атомов и энергии гидратации ионов. Чем меньше энергия сублимации и энергия ионизации и чем больше энергия гидратации, тем выше способность металла посылать ионы в раствор и тем ниже его равновесный потенциал. Из таких пассивных металлов, как медь, серебро, выход ионов в раствор почти не происходит. Поэтому, например, для медного электрода, погруженного в раствор соли меди, преобладает адсорбция ионов металла на поверхности электрода. [23]
Рассчитанные Элеем [4] теплоты хемосорбции газов на различных переходных металлах при допущении образования ковалентных связей М - X дают правильный порядок этих величин для многих газов. В этих расчетах особое значение придается теплоте сублимации металла и меньшее - вкладу частично ионного характера связи М - X, определяемому из дипольного момента хемосорбционной связи. [24]
Радиусы некайносимметричных 3s - и Зр-орбиталей, вытесненных псевдо-потенциалом из более глубоких положений, превышают радиусы Зе ( - орбита-лей, начиная с ванадия. Кайносимметрия Зс ( - атомов выражается и в пониженных ( по сравнению с 4d и 5d) энергиях сублимации металлов и в меньшей прочности образуемых ими комплексных соединений. [25]
Положение с энергией связи NiC может служить хорошим примером сложности подобных оценок. Если исходить из достаточно надежно установленной теплоты взаимодействия никеля с 4 молекулами окиси углерода ( 39 ккал / моль) и учесть теплоту сублимации металла ( 81 ккал / г-атом), то для газообразного состояния получим Ni 4СО Ni ( CO) 4 - - 120 ккал / моль. Отсюда энергия каждой связи Ni-С должна быть равна 120: 4 30 ккал / моль. [26]
Положение с энергией связи NIC может служить хорошим примером сложности подобных оценок. Если исходить из достаточно надежно установленной теплоты взаимодействия никеля с 4 молекулами окиси углерода ( 39 ккал / моль) и учесть теплоту сублимации металла ( 81 ккал / г-атом), то для газообразного состояния получим Ni - f 4CO № ( СО) 4 120 ккал / моль. Отсюда энергия каждой связи Ni-С должна быть равна 120: 4 30 ккал / моль. [27]
 |
Кинетическая кривая сублимации сплава магния с 5 15 / Zn и 0 5 % Zr при 350 С в вакууме 2 66 мкн / м1 2 - 10 - 8 мм рт. ст.. [28] |
Расчет показывает, что для удаления кислорода с поверхности вольфрамовой нити при 1200 С требуется несколько лет. Основная масса хемосорбиро-ванного водорода удаляется с поверхности металлов при 500 С, а кислород, хемосорбированный на никеле и железе, не десор-бируется в заметных количествах даже при температурах начала сублимации металла. Естественно полагать, что сохраняющиеся адсорбированные слои газа в условиях умеренного нагрева могут повлиять на испарение металла подобно тому, как они влияют на другое поверхностное явление - электронную эмиссию. [29]
В общем случае температурная зависимость давления насыщенного пара для твердых а - и р-кристаллов и жидкой фазы оказывается неодинаковой. Поэтому, естественно, что теплота сублимации ( испарения) в соответствующих этим участкам тем пературных интервалах также различна. Однако в преобладающем числе случаев сублимации металлов эти различия весьма незначительны и часто лежат за пределами точности измерения. [30]
Страницы: 1 2 3