Ароматический субстрат
Cтраница 2
При обработке некоторых ароматических субстратов формальдегидом и НС1 в кольцо вводится группа СН2С1 по реакции, которая носит название хлоре / метилирования. [16]
Атака Ra - исходного ароматического субстрата, таким образом, является скоростьлимитирующей стадией. Атака под действием НО - - гидроксилирование - особенно важна в биологических системах как первая стадия обезвреживания чужих ароматических молекул. Однако наиболее детально исследовано замещение атома водорода на арильную группу - арилирование. [17]
Реакции супероксид-иона с ароматическими субстратами, по-видимому, предшествует перенос электрона. Супероксид калия взаимодействует с л-нитрохлорбензолом в ГМФТА, давая 76 % л-нитрофенола. [18]
Далее арильный радикал атакует ароматический субстрат с образованием арилциклогексадиенильного радикала. [19]
Электрофильное металлирование с участием ароматических субстратов наблюдается при использовании, например, солей ртути, таллия и свинца. Эти реакции не следует смешивать с металлиро-ванием при участии, например, литийорганических соединений, таких как н-бутиллитий. В последнем случае реакция формально представляет собой отрыв наиболее кислого водорода ароматического субстрата н-бутил-анионом. [20]
В большинстве случаев выходы моноалкильных замещенных ароматических субстратов довольно низки, так как попутно образуется большое число других продуктов. Если из источника радикалов сначала получаются ацетокси-радикалы, то они могут входить в субстрат в виде сложпоэфирпой группы. Известно, что при действии тетраацетата свинца на нафталин образуются не метилнафталины, а только нафтилацетаты. Причина гораздо большей распространенности нежелательных реакций при ароматическом алкилирова-пии по сравнению с арилировапием заключается в том, что при введении алкильной группы вводится бензилышй водород, поэтому образующиеся алкильные радикалы расходуются на дегидрирование и последующее алкилирование боковой цепи. [21]
Дальнейшее взаимодействие карбкатионов с ароматическим субстратом идет по общей схеме электрофильного замещения через промежуточное образование а-комплексов. [22]
Этот комплекс реагирует с ароматическими субстратами аналогично ацилгалогенидам в реакции Фриделя - Крафтса. [23]
Дальнейшее взаимодействие карбкатионов с ароматическим субстратом идет по общей схеме электрофильного замещения через промежуточное образование а-комплексов. [24]
Этот комплекс реагирует с ароматическими субстратами аналогично ацилгалогеиидам в реакции Фриделя - Крафтса. [25]
Реакция азосочетания арилдиазония с высокоосновными ароматическими субстратами является типичной реакцией электрофиль-ного замещения, причем электрофильной частицей является диази-н Пйкатиин. [26]
Активной электрофильной частицей, атакующей ароматический субстрат при алкилировании, является алкил-катион в свободном виде или в форме ионной пары. Концентрация этих электрофиль-ных частиц зависит от тенденции галогенов к комплексообразова-нию с катализаторами Фриделя-Крафтса, которая падает с увеличением их объема от фтора к иоду. Поэтому алкилиодиды для алкилирования не используются. [27]
При использовании фенола в качестве ароматического субстрата в рассматриваемых реакциях не удается остановиться на стадии образования монозамещенного хлорметил - и соответственно оксилметилфенола, в данном случае образуются фенолфор-мальдегпдные смолы ( см. стр. [28]
Чтобы правильно объяснить влияние строения ароматического субстрата на скорость реакции замещения, необходимо установить, какая нз стадий процесса является смой медленной. [29]
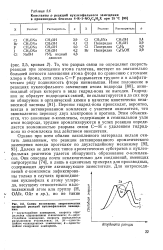 |
Схемы возможных энергетических профилей реакций нуклеофильного замещения. [30] |
Страницы: 1 2 3 4