Ароматический субстрат
Cтраница 3
Далеко не для всех типов ароматических субстратов и нуклео-фильных реагентов удается обнаружить образование о-комплек-сов. Они описаны почти исключительно для соединений, имеющих нитрогруппы [74], и лишь в единичных примерах для производных, содержащих другие активирующие заместители. [31]
К счастью, применение избытка ароматического субстрата подавляет образование продуктов нолиалкилировання. [32]
Чтобы правильно объяснить влияние строения ароматического субстрата на скорость реакции замещения, необходимо установить, какая из стадий процесса является самой медленной. [33]
Поэтому нуклеофил способен подойти к ароматическому субстрату с любой стороны плоского кольца. [34]
Хлориминиевая соль реагирует только с ароматическими субстратами, содержащими сильные электронодопорные группы NR2, NHR, OR, ОН. Продукт замещения - а-хлорамин гидролизуют до альдегида действием водного раствора ацетата натрия. [35]
Конденсация альдегидов и кетонов с ароматическими субстратами. [36]
Во всех рассмотренных выше иодирующих системах ароматический субстрат атакуется электррфилыюй иодирующей частицей. Однако субстратная селективность йодирования варьируется в широких пределах в зависимости от способа генерирования электрофильного иода и среды. Если в первой системе иодирующий агент проявляет высокую активность и низкую селективность, то в последних - низкую активность и высокую селективность. Различия обусловлены, очевидно, особенностями строения и сольватации атакующего злектрофила. Высказанные предположения о том, что в первом случае реагирует ацетил -, а в последних - - трифторацетил-гипоиодит ничего не объясняют, поскольку трифтора. [37]
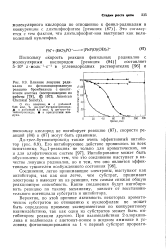 |
Влияние ловушек радикалов на фотоинициированную реакцию бромбензола с енолят-ионом ацетона ( воспроизведено из работы, 1973, American Chemical Society. [38] |
Вероятно, по этой причине активность некоторых ароматических субстратов по отношению к нуклеофилам не может быть определена прямыми экспериментами по конкурентному взаимодействию, так как один из субстратов может быть ингибитором реакции другого. [39]
Константы устойчивости л-комплексов очень слабо зависят природы ароматического субстрата. [40]
Скорость реакции определяется стадией присоединения радикала к ароматическому субстрату. [41]
Катион этой ионной пары, взаимодействуя с ароматическим субстратом, образует продукт алкилирования, радикал которого имеет разветвленное строение. [42]
В отличие от нитрования, при галогенировании атака ароматического субстрата может осуществляться различными электрофилами. Свободные галогены, например С12 и Вг2, могут легко атаковать активированное ароматическое ядро ( см. разд. [43]
При использовании в рассматриваемых реакциях фенола в качестве ароматического субстрата не удается остановиться на стадии образования монозамещенных хлорметил - и гидрокси-метилфенолов; в данном случае образуются фенолоформальде-гидные смолы. [44]
При использовании в рассматриваемых реакциях фенола в качестве ароматического субстрата не удается остановиться на стадии образования монозамещенных хлорметил - и гидроксн-метилфенолов; в данном случае образуются фенолоформальдегидные смолы. [45]
Страницы: 1 2 3 4