Субъединица
Cтраница 1
Субъединица формирует центр связывания антибиотиков ри-фампицина и стрептолидигина, являющихся специфическими ингибиторами бактериальных РНК-полимераз. Функция а-субъеди-ницы не известна. [1]
Субъединица ( 95 кДа) пронизывает мембрану насквозь и содержит на внутренней стороне участки для связывания АТФ и Na, а на внешней стороне - К и сердечных гликозидов. Субъединицы ( 40 кДа) содержат углеводные группы, расположенные на наружной стороне плазматической мембраны. Она способствует правильной ориентации фермента в липидном бислое. Перенос ионов происходит за счет изменения конформации фермента при его фрсфорили-ровании - дефосфорилировании за счет АТФ. [2]
Субъединица ВЦМ1) содержит центр связывания субстрата и окисляемые в р-ции группы 5Н, субъединица В2 ( М2) - кофактор ( представляет собой комплекс двух ионов Ре с неск. В состав кофактора входит также остаток тирозина, участвующий в восстановлении субстрата в свободиорадикальной форме. [3]
Субъединица Т.г. содержит две олигосахаридные цепи, р-одну. Олигосахаридные цепи присоединены к полипептидным цепям по остаткам аспарагина с помощью К-глико-зидных связей. В состав углеводной части, к-рая составляет 15 - 30 % от мол. О-маннозы, В-галактозы, Ь - фукозы, Н - ацетилглюкозамина, М - а цетил-галактозамина и, возможно, сиаловой к-ты. Углеводный состав а - и р-субъединиц различен. [4]
Субъединица Т.г. по первичной структуре, полипептидной цепи практически идентична а-субъединицам лютеини-зирующего гормона, фолликулостимулирунщего гормона, а также хорионического гонадотрошша той же видовой принадлежности. [5]
Субъединица может состоять из двух и более цепей, соединенных дисульфидными связями. [6]
Субъединица а - ХГ идентична а-субъединице лютеинизи-рующего гормона, фолликулостимулирующего гормона, а также тиреотропного гормона и включает 92 аминокислотных остатка. ХГ, полипептидная цепь к-рой состоит из 145 аминокислотных остатков, специфична для данного гормона, но проявляет высокую степень структурной гомологии ( ок. [7]
Субъединица формирует центр связывания антибиотиков ри-фампицина и стрептолидигина, являющихся специфическими ингибиторами бактериальных РНК-полимераз. Функция а-субъединицы не известна. [8]
Субъединица этого белка состоит в основном из семи параллельных или антипараллельных а-спира-лей, вытянутых от одной поверхности мембраны до другой. Другая хорошо исследованная система обсуждается ниже. [9]
Субъединица формирует центр связывания антибиотиков ри-фампицина и стрептолидигина, являющихся специфическими ингибиторами бактериальных РНК-полимераз. Функция а-субъединицы не известна. [10]
Субъединица этого белка состоит в основном из семи параллельных или антипараллельных а-спира-лей, вытянутых от одной поверхности мембраны до другой. Другая хорошо исследованная система обсуждается ниже. [11]
Субъединица, содержащая 96 аминокислотных остатков, ТТГ весьма консервативна и почти не имеет межвидовых различий. Биологическая активность ТТГ, как и других гликопротеиновых гормонов, определяется строением р-субъединицы ( 112 аминокислотных остатков), которая обеспечивает взаимодействие гормона с рецептором. Вместе с тем свободная р-субъединица неактивна и проявляет биологическую активность только в комплексе с а-субъединицей. По мнению ряда авторов, а-субъедини-ца является не только активатором, но и протектором р-субъединицы от действия протеиназ. [12]
Субъединица ФСГ и трех др. родственных гормонов кодируются одним геном, Р - ФСГ - отдельным геном. В процессе биосинтеза вначале синтезируется на отдельных матричных РНК полипептидная цепь каждой из субьединиц. Синтез и присоединение олигосахаридных цепей происходят в процессе трансляции субъединиц и после ее завершения. Во время котрансляционного гликозилирования богатые ман-нозой олигосахаридные фрагменты присоединяются к остаткам аспарагина. При этом может происходить сульфирование концевых остатков гексозаминов. [13]
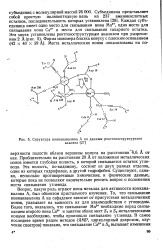 |
Структура конканавалина А по данным рентгеноструктурного. [14] |
Каждая субъединица имеет одно место для связывания иона Мп2, одно место для связывания иона Са2 и место для связывания сахарного остатка. [15]
Страницы: 1 2 3 4